Сахарный диабет является одним из самых распространенных хронических заболеваний: согласно подсчётам, в мире более 100 миллионов людей страдают этим тяжелым недугом. Например, в Российской Федерации зарегистрировано более 2 миллионов больных сахарным диабетом, в том числе более 300 тысяч инсулинозависимых. Однако, по результатам различных эпидемиологических исследований, реальное количество больных составляет более 8 миллионов человек [1,2,3]. Сходная картина наблюдается и в Республике Казахстан [4,5].
Поэтому разработка и внедрение новых высокоэффективных способов лечения данной патологии является в настоящее время весьма актуальной.
Для воспроизведения сахарного диабета была использована модель аллоксанового диабета осуществляемая посредством введения в хвостовую вену крысы моногидрата аллоксана в виде 5% раствора в дистиллированной воде, из расчёта 40 мг/кг [6]. Данная модель позволяет получить биохимическую картину заболевания на 4-6 сутки после введения и стойкую гипергликемию не менее 4-6 недель. Во время эксперимента животные содержались на стандартной виварной диете.
На 14-е сутки после создания модели аллоксанового диабета животным внутри брюшинно вводились островковые клетки фетальной поджелудочной железы в объёме 1,0 мл физиологического раствора в количестве 2х106.
Морфологическая оценка состояния поджелудочной железы у животных с экспериментальным аллоксановым диабетом до и после введения фетальных островковых клеток поджелудочной железы.
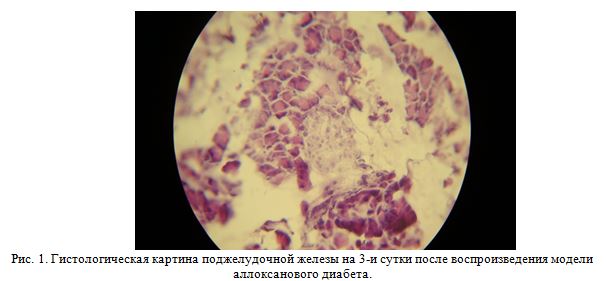
Анализ полученных данных показал, что на препарате поджелудочной железы на третьи сутки после введения алоксана (рисунок 1) выявляется резко выраженная картина дистрофии и некроза паренхимы и стромы поджелудочной железы. Отмечается обширный некроз инсулярного аппарата железы. Структура ацинусов нечёткая, выявляется гиперхромия ядер.
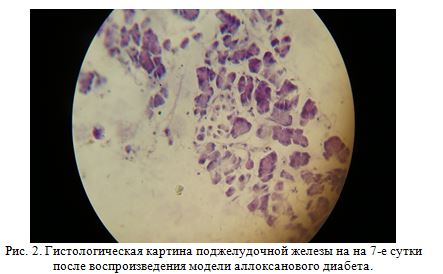
В гистологическом препарате поджелудочной железы на седьмые сутки после воспроизведения модели алоксанового диабета (рис. 2) отмечается расширение зоны некроза, выявляются очаговые зоны сохранившихся ацинусов и инсулярного аппарата. В поле зрения отмечается картина очищение очага некроза.
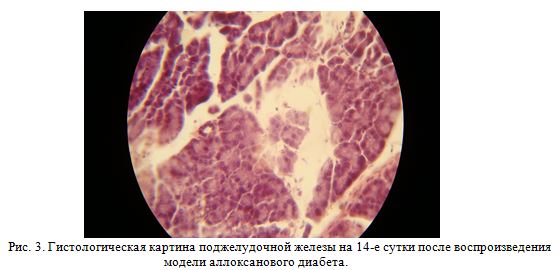
Гистологическая картина поджелудочной железы на четырнадцатые сутки от начала эксперимента по воспроизведению модели диабета в поджелудочной железе (рис. 3) показывает частичного восстановления ацинусов и островков. Однако их структура слабо выражена и неоднородна. В результате обширного некроза и дистрофии отмечается резкое истончение паренхимы и обширное разрастание соединительной ткани.
На фоне выявленных морфологических изменений поджелудочной железы после воспроизведения экспериментальной модели алаксанового диабета. Было осуществлено внутрибрюшинное введение фетальных островковых клеток поджелудочной железы после культивирования и криоконсервирования в условиях in vitro.
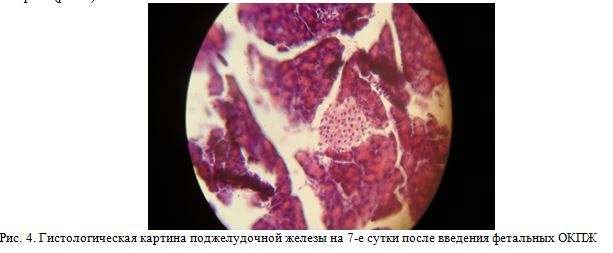
На седьмые сутки после введения фетальных клеток отмечается резко выраженное увеличение массы клеток. Выявляются вновь формирующиеся ацинусы среди которых множество островковых клеток (рис. 4).
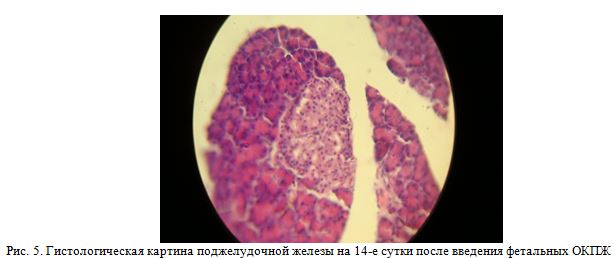
На четырнадцатые сутки после введения фетальных островковых клеток поджелудочной железы гистологически отмечается хорошо выраженная тина паренхимы ацинуса и островковых желез. В средине сформированного ацинуса выделяется структура содержащая до несколько сот клеток островкового аппарата (рис. 5).
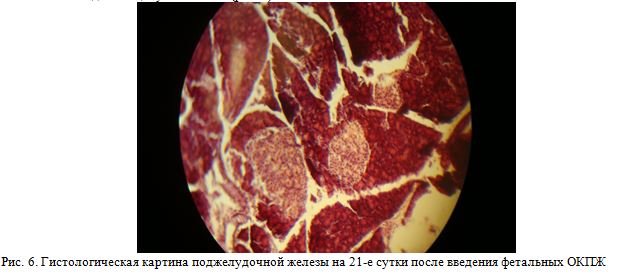
На 21-е сутки после имплантации клеток усиливаются процессы регенерации ацинусных и инсулярных структур. В одном поле зрения встречаются 3-4 организованных структуры инсулярного аппарата и множество долек ацинусных желез (рис. 6).
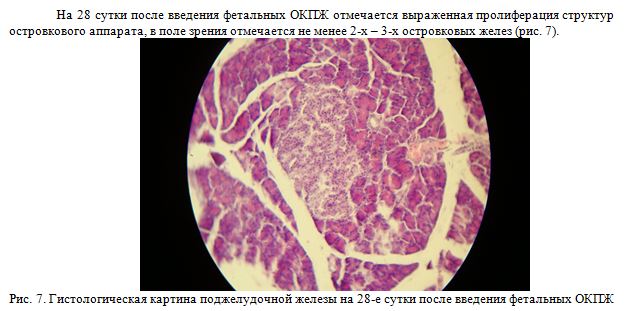
На 28 сутки после введения фетальных ОКПЖ отмечается выраженная пролиферация структур островкового аппарата, в поле зрения отмечается не менее 2-х – 3-х островковых желез (рис. 7).
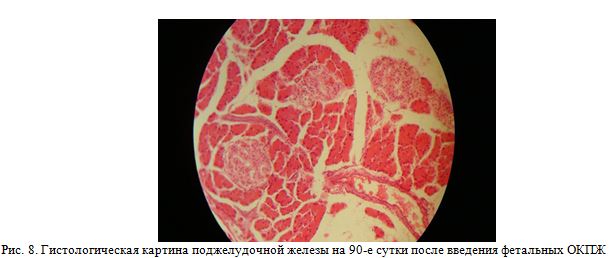
Через 90 дней после введения островковых клеток фетальной поджелудочной железы отмечено полное формирование структуры поджелудочной железы (рис. 8).
Таким образом, применение фетальных островковых клеток поджелудочной железы при лечении экспериментального сахарного диабета позволяет в течение трёх месяцев восстановить морфологи-ческую структуру поджелудочной железы экспериментальных животных. Данное обстоятельство позволяет предположить эффективность клинического применения фетальных клеток при лечении диабета у людей.
Литература
- Дедов И.И., Шестакова М. В. Сахарный диабет. – Москва, 2003. – 455 С.
- World Health Organization International Diabetes Federation Europe. Diabetes care and research in Europe: the St Vincent Declaration. // Diabet Med.- 1990. – Vol. 7. – P. 360.
- R. Paul Robertson. Islet Transplantation as a treatment for diabetes – a work in progress. – A New Therapeutic Concept // N. Engl. J. Med. – August, 7, 2003. – Vol. 350. – P. 694-705.
- Зельцер М. Е. Сахарный диабет в Казахстане как медико-социальная проблема. // Здравоохранение Казахстана. – 1994 г. - № 9. – С. 44-45.
- Зельцер М. Е. Изучение эпидемиологии сахарного диабета в Казахстане. // Материалы 1 конгресса диабетологов Центральной Азии. – Алматы, 1994
- Вельбри С.К. Иммунологическая диагностика заболеваний поджелудочной железы – М., Медицина, 1985. – 136 с.