Принято считать, что мочеиспускание у ребенка - произвольный, сложный рефлекторный акт, во время которого должно произойти синхронное расслабление сфинктеров мочевого пузыря и сокращение детрузора. Его осуществление обеспечивается системой нервных структур, регулирующих и контролирующих функциональное состояние мочевого пузыря, поэтому нормальное мочеиспускание возможно при анатомической и функциональной полноценности не только сфинктеров и детрузора, но и нервных центров и проводников [1, 2]. Физиологии мочеиспускания посвящено большое количество научных работ и клинических наблюдений, имеющих значение для понимания механизмов и причинно-следственных взаимосвязей возникновения нейрогенных функциональных нарушений мочевого пузыря. Однако, необходимо отметить, что по некоторым вопросам в литературе встречаются порой разноречивые мнения [3, 4].
Ряд работ посвящено путям корковой регуляции функции мочевого пузыря, указывающий, что кортикальные импульсы передаются по срамному нерву к поперечнополосатому наружному сфинктеру, вызывая его расслабление, а это в свою очередь, путем спинального рефлекса ведет к сокращению детрузора и расслаблению внутреннего гладкомышечного сфинктера [5, 6]. По мнению Бадаляна Л.О. (1985) имеют значение следующие основные нервные структуры, регулирующие акт мочеиспускания: периферические рецепторы симпатических и парасимпатических нервов мочевого пузыря; симпатические центры, расположенные в сегментах L2-L4 спинного мозга (повышение тонуса симпатических структур ведёт к сокращению сфинктеров и расслаблению детрузора, то есть к удержанию мочи, торможению акта мочеиспускания); парасимпатические центры, находящиеся в сегментах s2-s4 (возбуждение парасимпатических структур вызывает расслабление сфинктеров и сокращение детрузора, то есть опорожнение мочевого пузыря); центральные вегетативные центры участвующие в регуляции мочеиспускания, расположенные в продолговатом мозгу и гипоталамической области; чувствительные волокна от наружного сфинктера, идущие по боковым и задним столбам спинного мозга к коре больших полушарий (парацентральная долька теменной области и передняя центральная извилина); корковые центры, регулирующие произвольный акт мочеиспускания [7].
Папаян А.В. (1998) условно выделяет три «этажа» нервной регуляции мочевого пузыря, каждый из которых имеет определенную функциональную самостоятельность, но подчиняется верхнему [8]. Первый этаж представлен соединением нейрона с пучком гладких мышечных волокон детрузора, которые могут иметь адренергическую или холинергическую структуру. Наружный сфинктер мочеиспускательного канала, состоящий из поперечнополосатой мускулатуры, функционирует произвольно. Он иннервируется альфа- мотонейронами передних рогов 2-4 сакральных сегментов спинного мозга. Волокна этих клеток входят в состав срамных нервов (n. pudendi) и осуществляют соматическую иннервацию наружного уретрального сфинктера и мышц тазового дна. Второй этаж регуляции представлен спинальными центрами мочеиспускания: симпатическая иннервация осуществляется клетками Якобсона, расположенными в боковых рогах серого вещества спинного мозга на уровне 12-го грудного — 2-го поясничного сегментов. Симпатические преганглионарные волокна выходят из спинного мозга в составе передних корешков и заканчиваются в поясничных узлах симпатического ствола. Постганглионарные волокна формируют подчревные нервы (n. hypogastrici), которые вместе с парасимпатическими волокнами образуют пузырное сплетение, а заканчиваются в мышечном слое мочевого пузыря и внутреннем сфинктере уретры. Парасимпатическая иннервация осуществляется ядрами ii-iv крестцовых сегментов, расположенных в конусе спинного мозга. Волокна от этих ядер покидают спинной мозг в составе передних корешков, затем образуют тазовые нервы (n. pelvici), которые частично заканчиваются в пузырном сплетении, частично в интрамуральных ганглиях.
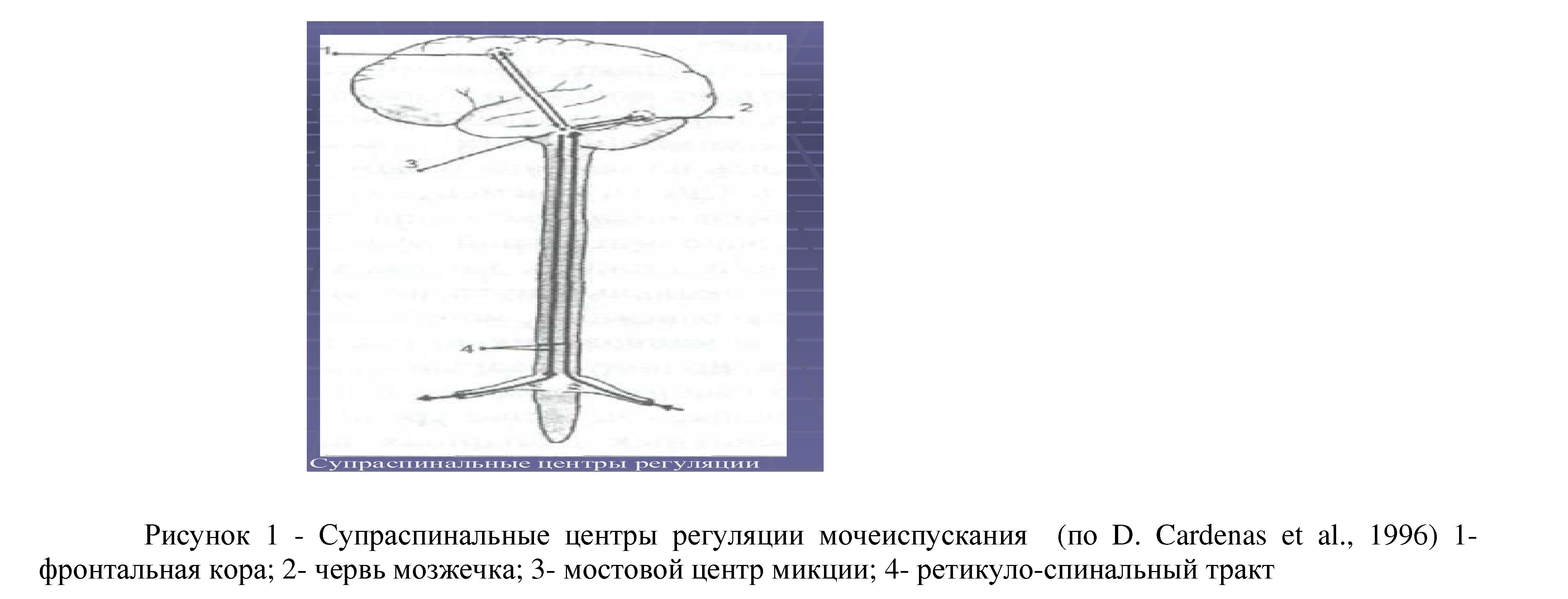
Третьи этаж или высший уровень регуляции мочеиспускания составляют надсегментарные центры, которые располагаются в Варолиевом мосте, гипоталамусе, среднем мозге, лобной и теменной долях головного мозга (Рис. 1).
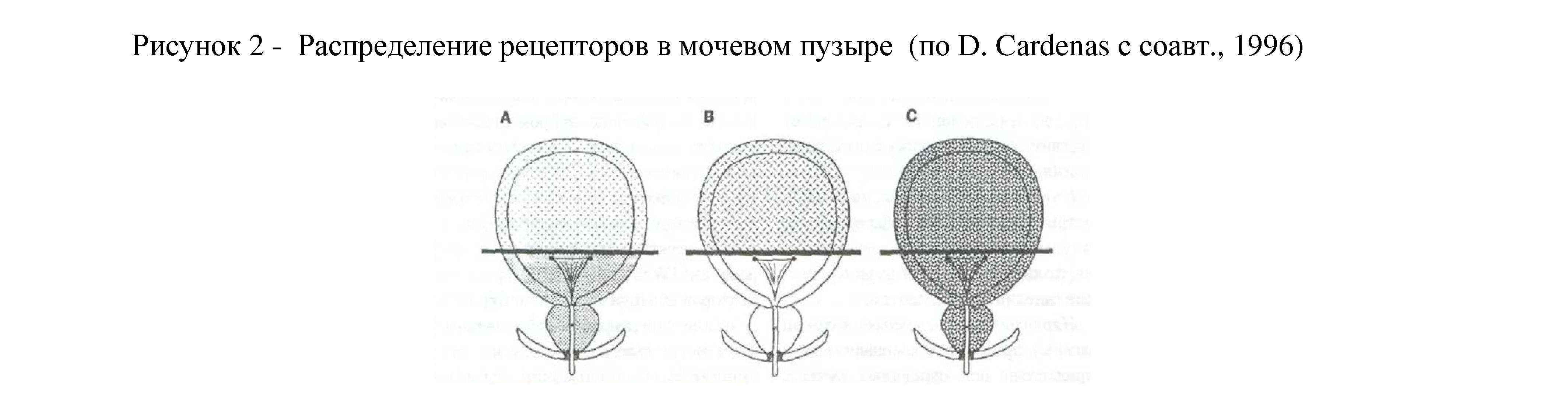
Функция нижних мочевыводящих путей регулируется и такими отделами центральной нервной системы, как специфические ядра зрительных бугров, нейрональные структуры червя и полушарии мозжечка, ретикулярная формация спинного и головного мозга [9]. Роль корковых и подкорковых центров мочеиспускания состоит в стимуляции или, что чаще наблюдается, торможении спинальных рефлексов мочеиспускания. Эфферентные импульсы в данном случае проводятся по пирамидальному тракту, ретикулоспинальным и проприоспинальным путям. Важную роль в регуляции функции мочевого пузыря играет и вегетативная нервная система. Мочевой пузырь имеет двойную (симпатическую и парасимпатическую) иннервацию. Известно, что ганглионарные клетки обоих видов вегетативной нервной системы сконцентрированы в области дна мочевого пузыря и начального отдела уретры. Кроме того, доказано существование адренергических нервных окончаний в парасимпатических тазовых нервных структурах, чем, очевидно, и обеспечивается автоматизм мочеиспускания при полной денервации мочевого пузыря [10, 11, 12]. Рецепторы вегетативной нервной системы распределены по внутренней поверхности мочевого пузыря неравномерно: симпатические располагаются преимущественно в области шейки, а парасимпатические — в области тела (Рис. 2).
А - распределение альфа - адренергических рецепторов (большая часть расположена в основании мочевого пузыря и предстательной железе) Б - распределение бета - адренергических рецепторов (большая часть локализована в куполе мочевого пузыря) В - распределение холинергических рецепторов (широко представлены в куполе, и в основании мочевого пузыря и в уретре)
Функциональный эффект раздражения симпатической нервной системы зависит от характера взаимодействия норадреналина с альфа- и бета-адренорецепторами, который оказывается противоположным. При взаимодействии с норадреналином альфа-рецепторы, которые локализованы в области гладкомышечного сфинктера задней уретры и шейки мочевого пузыря, вызывают их сокращение, то есть обеспечивают удержание мочи в период накопления. Этой же цели подчинено взаимодействие норадреналина с бета- рецепторами симпатических волокон, расположенных в области тела мочевого пузыря, вызывающее расслабление гладкомышечных волокон детрузора. Определенное значение для взаимодействия имеет и концентрация норэпинефрина. Так, альфа-адренорецепторы чувствительны к высокой концентрации, а бета- адренорецепторы — к более низкой концентрации этого медиатора. Парасимпатические волокна вегетативной нервной системы также имеют два вида рецепторов: мускариночувствительные — M- холинорецепторы, расположенные у окончания постганглионарных парасимпатических волокон и в центральной нервной системе; никотиночувствительные репепторы (Н-холинорецепторы), сконцентрированные в вегетативных ганглиях, мозговом веществе надпочечников и скелетной мускулатуре M-холинорецепторы, при этом M- холинорецепторы при взаимодействии с ацетилхолином оказывают на детрузор сокращающее действие [9]. В случае нарушения иннервации мочевого пузыря независимо от характера первичных факторов, вызывающих эти расстройства, активизируются его резервуарная и эвакуаторная функции.
В постнатальном периоде структурно-функциональной организации мочевого пузыря и мочеиспускания имеется ряд особенностей [13]. В частности мочевой пузырь у новорожденного является внутрибрюшным органом. В течение первых 1,5-2 лет жизни мочевой пузырь опускается и основная его часть становится внутрибрюшинной, а сам орган в основном тазовым. Причем эффективный объем этого органа у новорожденного в 4 раза меньше, чем у 4-летнего ребенка, соединительнотканные структуры стенки мочевого пузыря у новорожденного относительно более развиты, чем у детей старшего возраста, что связано с возрастными закономерностями его формирования. В первые дни жизни новорожденного, поскольку мочи мало, редко отмечается за сутки более 4-6 мочеиспусканий. Начиная с третьих суток жизни число мочеиспусканий быстро увеличивается и к концу первой недели может достигать 20-25. К концу первого года жизни число мочеиспусканий снижается до 14-15, к 2-3 годам до 10. Нормативные показатели суточного позывного ритма и объема мочевого пузыря у детей разного пола и возраста приведены в таблице 1.
Таблица 1 - Усредненные показатели ритма спонтанных мочеиспусканий и эффективной емкости мочевого пузыря у детей (Осипов И.Б., Смирнова Л.П., 2001)
|
Возраст |
Частота |
моче- |
Эффективный объем мочевого |
Минимальные |
и |
максимальные |
|
(лет) |
испусканий в сутки |
пузыря (мл) |
значения объема мочевого пузыря |
|||
|
Девочки |
Мальчики |
|||||
|
4-7 |
6 |
120 |
68-190 |
63-135 46- |
||
|
8-11 |
5 |
150 |
50-235 115-270 |
270 39-325 |
||
|
12-14 |
4 |
200 |
||||
Несмотря на очевидные различия структуры и функций пищеварительной и мочевыделительной систем, можно найти немало общего в плане их структурно-функциональной организации [14, 15]. Нижние мочевые пути и толстая кишка имеют тесную анатомо-функциональную связь за счет схожего эмбрионального происхождения, иннервации, кровоснабжения, как эндокринной, так и нейрональной (спинномозговой и корковой) регуляции функций. Мочевой пузырь и прямая кишка имеют похожее предназначение (адаптации, эвакуации, замыкания), которые обеспечиваются однотипными рефлексами. Иннервация мышц, изгоняющих мочу и каловые массы, и мышц, их удерживающих (уретральные и анальные сфинктеры), во многом одинакова, из-за тесной анатомической связи и схожие физиологические функции мочевого пузыря и прямой кишки. Нервные волокна к этим органам проходят в составе подчревного (симпатические волокна), тазового (парасимпатические) и срамного (соматические) нервов. Центры вегетативной нервной системы, регулирующие акты мочеиспускания и дефекации, расположены в поясничных и крестцовых сегментах спинного мозга [16]. Возбуждение парасимпатических волокон, исходящих из средних крестцовых сегментов (S2—S4), приводит к сокращению детрузора мочевого пузыря и продольной мускулатуры нисходящей, сигмовидной и прямой кишок и одновременному расслаблению их внутренних (безусловных) сфинктеров.
Поэтому можно сказать, что парасимпатическая система отвечает за выполнение актов мочеиспускания и дефекации. Напротив, раздражение симпатических нервов, отходящих от верхних поясничных сегментов (L1 - L2), способствует удержанию мочи за счет расслабления детрузора и континенции кала вследствие торможения моторики продольного мышечного слоя нисходящей, сигмовидной и прямой кишок и возбуждения сокращений внутренних сфинктеров. Сокращение наружных сфинктеров может возникать как рефлекторно под влиянием сигналов, поступающих в спинной мозг по афферентным волокнам тазовых нервов, так и за счет супраспинальной активации соматических эфферентов в S2—S4 [14, 15]. За осуществление анальной континенции во время акта мочеиспускания отвечает внутренний сфинктер заднего прохода, в то время как электрическая активность наружного сфинктера полностью подавляется (пузырно-анальный рефлекс) [17].
Только скоординированная работа афферентных и эфферентных звеньев как вегетативной, так и соматической нервных систем позволяет осуществлять основные предназначения тазовых органов: удержание мочи и кала (резервуарная функция) и их удаление (эвакуаторная функция). Существуют и некоторые различия в нервной регуляции актов мочеиспускания и дефекации. Хотя мочеиспускание и является автоматическим рефлекторным процессом, на него оказывают влияния вышележащие отделы головного мозга, включая кору больших полушарий. Эти влияния носят преимущественно тормозной характер, обеспечивающий реализацию акта мочеиспускания только в надлежащих условиях окружающей обстановки. Именно наружному сфинктеру уретры принадлежит ключевая роль в процессе произвольного удержания мочи. В норме постоянная тоническая активность этой мышцы ответственна за рефлекторное сжатие уретры и предотвращает ее открытие при сокращении волокон m. levator ani во время напряжения. Рефлекторные сокращения леватора обеспечивают эффективное предотвращение опущения шейки мочевого пузыря и повышают внутриуретральное давление во время резкого подъема внутрибрюшного давления.
Очевидно, что нормальные микционный и дефекационный циклы невозможны без адекватного синхронного сокращения и расслабления мышц тазового дна, которое представляет собой сложное мышечносоединительнотканное образование [18]. Тазовое дно активно участвует в волевом и рефлекторном удержании и эвакуации мочи и кала. Патология тазового дна часто проявляется двумя синдромами — относительной недостаточности выхода и относительной обструкции выхода. Без сокращения или расслабления тазового дна невозможно оптимальное функционирование тазовых органов. Расслабляясь и сокращаясь, мышцы тазового дна регулируют опущение и подъем тазового дна и степень взаимодействия выводящих каналов (уретры и анального канала) с абдоминальным давлением. Обеспечивает оптимальную трансмиссию брюшного давления на резервуар и каналы, являющиеся основным механизмом в удержании и эвакуации мочи и кала. Хотя недержание мочи и недержание кала имеют различные причины возникновения, с патогенетической точки зрения эти расстройства родственны между собой, поскольку в их основе лежит одно и то же нарушение — дисфункция мускулатуры тазового дна [14, 18].
Таким образом, нарушение мочеиспускания и дефекации являются двумя из наиболее тяжелых проявлении врожденных пороков развития позвоночника и спинного мозга и зачастую именно они определяют тяжесть состояния ребенка, а следовательно и степень его дезадаптации. Регуляция резервуарно - эвакуаторной функции мочевого пузыря и прямой кишки осуществляется посредством сочетанных действий парасимпатического, симпатического и соматического нервных аппаратов, расположенных в различных отделах спинного мозга, принадлежащих различным медиаторно-синаптическим системам. Степень повреждения этих структурно-функциональных составляющих участвующих в осуществлении тех или иных тазовых функций (резервации мочи, накопления кала, эвакуации мочи, выделения кала и др.) при спинальных дизрафиях в зависимости от особенностей поражения спинного мозга и корешков отличаются, а чувствительность симпатических, парасимпатических и соматических структур к растяжению, гипоксии, сдавлению и другим патогенетическим воздействиям различные.

Поэтому выраженность и течение тазовых расстройств отличаются при тех или иных формах врожденных пороков развития и зачастую различные у разных больных. Учет этих анатомо-функциональных особенностей, в том числе и их динамики в процессе роста ребенка, необходимы для правильного распознавания заболевания, прогнозирования течения и определения оптимальной тактики лечения порока развития нервной системы. Физиология мочеиспускания является сложной по структурно-функциональной организации и ее параметры меняются в постнатальном периоде, особенно в течение первых 1-3 лет жизни. Эволюция этой функции при врожденных пороках развития иная чем в норме и учитывается в диагностическом процессе. Расстройства мочевыделения имеют многозвеньевое, сложное строение, клинически проявляются в отдельных возрастных группах по разному. Нарушения мочеиспускания и его эффективная коррекция во многом определяют успех лечения спинальных дизрафий. Современные тенденции оценки уродинамических нарушении при спинальных дизрафиях сводятся, в частности, к учету анотомо-физиологических особенностей реализации этой функции в разных возрастных группах при тех или иных формах этой аномалии развития.
ЛИТЕРАТУРА
- Банников В.M., Рункова М.В. Нейрогенные дисфункции мочевого пузыря. - M., 2004.
- Hampel C., Wienhold D., Benken N. et al. Definition of overactive bladder and epidemiology of urinary incontinence //Urology. - 1997. - V.50. - P.4-17.
- Крупин В.Н., Белова А.Н. Нейроурология: руководство для врачей. - M.: Антидор, 2005. - 464 с.
- Feneley R.C., Shepherd A.M., Powell P.H., Blannin J. Urinary incontinence: prevalence and needs //Br. J. Urol. - 1979. - V.51. - P.493-496.
- Holzbeierlein J., Pope J.I., Adams M.C. et al. The urodynamic profile of myelodysplasia in childhood with spinal closure during gestation //J. Urol. - 2000. - V.164. - P.1336-1339.
- Keating M.A., Rink R.C., Bauer S.B. et al. Neurourological implications of the changing approach in management of occult spinal lesions //J. Urol. - 1988. - V.140. - P.1299-1301.
- Бадалян Л.О. Детская неврология. - M., «Медицина». 1984. - С. 352-354.
- Папаян А.В. Энурез у детей /под ред. академика Ю.В. Наточина. - СПб., 1998. - С. 80.
- Cardenas D., Mayo M., King J. Urinary tract and bowel management in the rehabilitation setting // In: R. Braddon (ed) Physical Medicine and Rehabilitation. - W. B. Saunders Company. - 1996. - P. 555-579
- McGuire E. J., Bloom D. A., Ritchey M. L. Myelodysplasia // Prob. Urol. - 1993. - Vol. 7 - P. 7 - 11.
- Sureshkumar P., Craig J.C., Roy L.P., Knight J.F. Daytime urinary incontinence in primary school children: a population-based survey //J. Pediatr. - 2000. - V.137. - P.814-818.
- Boemers T.M. Urodynamic evaluation of children with the caudal regression syndrome (caudal dysplasia sequence). / Boemers T.M., Van Gool J.D., de Jong T.P., Bax K.M. // J. Urol. - Baltimor. - 1994. - Vol. 151. № 2. - P. 1038 - 1040.
- Осипов И.Б., Смирнова Л.П. Нейрогенный мочевой пузырь у детей. - Санкт-Питербург, «ПИТЕР». 2001. - 79 с.
- Лаптев Л.А. Нейродисфункции тазовой диафрагмы в генезе расстройств функций органов кало- мочевыделения у детей при миелодисплазии: Автореф. дис. д-ра мед. наук. - M., 1998. - 31 с.
- Кольбе О.Б., Сазонов А.Н., Моисеев А.Б. с соавт. Сочетанные нарушения функций мочевого пузыря и толстой кишки у детей // Педиатрия. - 2003. - 6. - C. 91-94.
- Зенков Л.Р., Ронкин М.А. Функциональная диагностика нервных болезней. 3-е изд., переработан. и дополн. - M.: МЕДпресс-информ., -2004. - 488 с.
- Sangwan Y.P. Fecal incontinence // Anorectal surdery. - 1994. - Vol. 74 (6). - P. 1377-1398.
- Салов П.П. Нейрогенные дисфункции тазовых органов. - Новокузнецк, 2002. - 592 с.