Аннотация
При расчете вероятностного критерия пкр был учтен статистический вес признака. Это позволило получить достоверные данные о присутствия бетулина в отдельных фракциях этанольного экстракта коры березы. Вывод о присутствии компонента подтвержден результатами тонкослойной хроматографии. Сделан вывод о возможности достоверной идентификации компонента в смеси по данным ИК-спектроскопии.
Контроль качества на всех этапах разработки и производства новых лекарственных препаратов, поливитаминных комплексов и пищевых добавок и задачей. Предлагаются новые способы определения и/или методов обработки др. является приоритетной совершенствования методик экспериментальных данных.
Спектрофотометрия является методом, использование которого одобрено национальными фармакопеями. Для подтверждения подлинности препарата, контроля за посторонними примесями, количественного определения веществ используется спектрофотометрия в ПК- области. Методы ИК-спектроскопии также могут быть успешно использованы для анализа многокомпонентных смесей органических соединений.
При фармацевтическом и биомедицинском анализе веществ возникает необходимость идентификации и разделения структурно близких аналогов. Эта же задача стоит при контроле синтеза лекарственных препаратов, разделении экстрактов из растительного сырья.
Возможность использования хемометрических подходов при анализе многокомпонентных смесей растительного происхождения по данным HK- спектроскопиибыла реализована при работе с растительными экстрактами (густая субстанция масла тополя бальзамического «Тополин» [1], экстракт тритерпеновых соединений коры березы).
Кора деревьев семейства березовых является богатейшим источником тритерпеноидных соединений ряда лупана - бетулина, лупеола, бетулиновой кислоты и Р-амирина. Основным тритерпеноидным соединением березы является пентациклический спирт - бетулин. Его содержание в бересте зависит от вида растения и может составлять до 25 % сухого веса [2]. Тритерпеновые соединения обладают широким спектром биологического действия, в частности они, оказывают противовоспалительную, антисклеротическую, желчегонную, антиаллергическую, противоопухолевую, противовирусную, антифунгицидную [3,4], а также с учетом новых разработок и анти-вич-активность [5], противотуберкулезное действие [6,7]. Примечательным является низкая токсичность данных соединений.
Объект исследования - сложные многокомпонентные смеси растительного происхождения - последовательно полученные фракции коры березы (Betulapendula и Betulapubescens). Растворитель и природа извлекаемых им соединений приведена в Таблице 1.
Последовательная экстракция сырья массой 12,13 г растворителями с повышающейся полярностью проведена в аппарате Сокслета, время экстрагирования - 5 суток, объем растворителя на каждом этапе составлял 350 мл.
Фракции получены различными способами: индивидуальная экстракция растворителем, по классической схеме - последовательная экстракция растворителями с повышающейся полярностью и по обратной схеме - последовательная экстракция растворителями с понижающейся полярностью.
Таблица 1 Классы соединений, экстрагируемые растворителями с различным градиентом полярности
|
Растворитель |
Температура кипения, 0C |
Полярность, 8г |
Извлекаемый класс соединений |
|
Гексан (CeHi4) |
68,7 |
31,0 |
Липиды |
|
Дихлорэтан (C2H4Cl2) |
83,5 |
38,1 |
Флавоноиды (агликоны), стерины |
|
Этилацетат (CH3COOC2H5) |
77,1 |
40,7 |
Карбоновые кислоты, эфиры |
|
Этанол (C2H5OH) |
78,3 |
51,7 |
Фенольные соединения, флавоноиды (гликозиды) |
В зависимости от природы растворителя, внешний вид полученных фракций отличался по цвету и консистенции (Таблица 2).
Таблица 2 Внешний вид осадков разных фракций
|
Фракции |
Масса осадка, г |
Внешний вид |
|
01.01.0 |
0,21 |
кристаллический порошок белого цвета |
|
02.01.0 |
0,63 |
кристаллический порошок белого цвета |
|
03.01.Р |
0,75 |
кристаллический порошок желтоватого цвета |
|
01.02.Р |
2,41 |
кристаллический порошок белого цвета |
|
01.03.P |
0,19 |
кристаллический порошок светло-коричневого цвета |
|
01.04.Р |
2,15 |
темно-коричневые кристаллы |
Примечание: первая цифра (например, 02) означает порядковый номер фракции; вторая - порядковый номер растворителя (01 - гексан, 02 - дихлорэтан, 03 - этилацетат, 04 - этанол); 01.0 - осадок, полученный в результате экстрагирования первым растворителем; 04.P - осадок, полученный в результате отгонки четвертого растворителя.
Для подтверждения достоверности полученных результатов проведена идентификация тритерпеновых соединений методом тонкослойной хроматографии (TCX) во всех исследуемых фракциях.
Хроматографирование проводили на пластинках «Sorbfil», в качестве растворителя использовался хлороформ, в качестве проявителя - 10 % - спиртовой раствор фосфорномолибденовой кислоты. Нагревание полученных хроматограмм проводилось до 120 0C. В качестве метчиков использовали бетулин, смесь бетулина с лупеолом (все вещества предварительно тщательно очищены многократной перекристаллизацией). Бетулин дает пятна тёмно-синего цвета.
В результате элюирования упаренного этанольного экстракта неполярными и слабополярными растворителями выделены вещества терпеновой и тритерпеновой природы, а элюирования спиртами - вещества полифенольной природы.
Для получения ИК-спектров использовались кристаллические фракции. Масса исследуемой системы колебалась в пределах от 5 мг до 0,5 мг, при общей массе навески 300 мг. Необходимым требованием использования вероятностных критериев является наличие эталонных ИК-спектров определяемых веществ.
Поэтому, получены ИК-спектры бетулина при различной концентрации индивидуального компонента, отвечающие требованиям спецификации Международного общества Кобленца [8].
ИК-спектры фракций снимались на ИК Фурье-спектрометре ФСМ-1201 в области для модификации 400 - 5000 см-1, при спектральном разрешении для модификаций не более 1.0 см-1, абсолютная погрешность градуировки шкалы волновых чисел составляла не более ±0,1 см-1.
Первым этапом исследования спектроскопических данных был расчет значения пкр без учета относительной интенсивности линий. Для этого сначала для идентификации индивидуальных веществ проведен предварительный отбор ИК-спектров исследуемых проб по наличию в них наиболее интенсивных пиков определенного эталона: три из пяти наиболее интенсивных пиков (Таблица 3).
|
Вещество |
Пик 1, см 1 |
Пик 2, см 1 |
Пик 3, см 1 |
|
Бетулин (Б) |
2941,79 |
1456,18 |
1029,98 |
Таблица 3 Волновое число наиболее интенсивных пиков ИК-спектра бетулина
Спектр смеси считался пригодным для дальнейшей работы при условии, что в нем присутствовало одновременно три линии, соответствующие одному индивидуальному веществу. Спектры, не отвечающие этому условию, были отбракованы, расчет статистических показателей для них не проводился.
Далее была рассчитана единичная вероятность случайного совпадения линий ИК-спектра эталонного вещества в ИК-спектре исследуемой пробы [8]. Значение этой величины рассчитано по эталонному ИК - спектру. Для расчета этой величины были использованы следующие значения: //-число линий в эталонном спектре; Al-максимальная погрешность измерения положения линий, данное значение определяется по прибору (для ФСМ - 1201 это значение равно 1 см-1); Ii - начало интервала, в котором проводилось сопоставление линий (400 см-1); X2 - конец интервала, в котором проводилось сопоставление линий (3000 см-1). Число линий в эталонном ИК-спектре Һ выдавала программа Fspec (Рисунок 1), где черным цветом показаны линии подсчитанные программой Fspec.
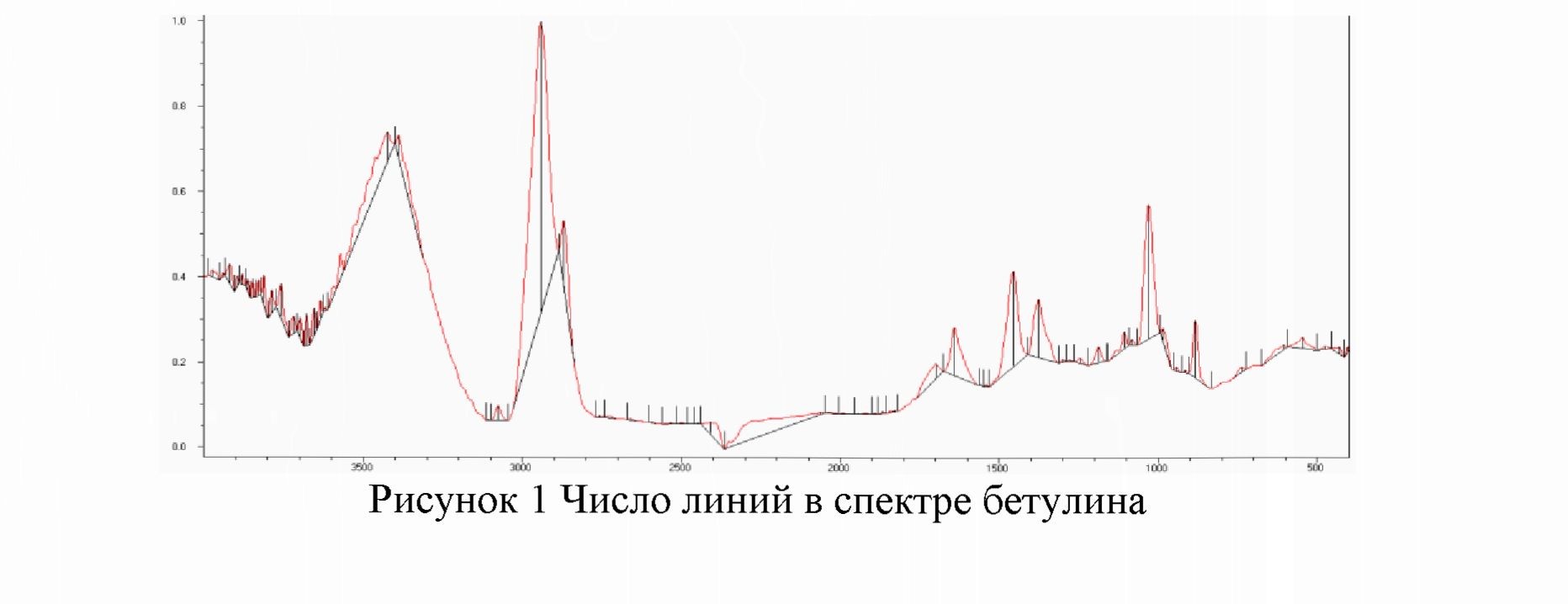
Для спектров, прошедших предварительный отбор по Формуле (1) была рассчитана P - единичная вероятность случайного совпадения.
Число линий в спектрах эталонных веществ и вероятность случайного совпадения линии Р. представлена в Таблице 4.
|
Эталонное вещество |
Число линий в спектре вещества, А |
Вероятность случайного совпадения линии, P |
|
Бетулин(Б) |
10 |
0,007 |
Таблица 4 Единичная вероятность случайного совпадения линии в ИК-спектрах бетулина
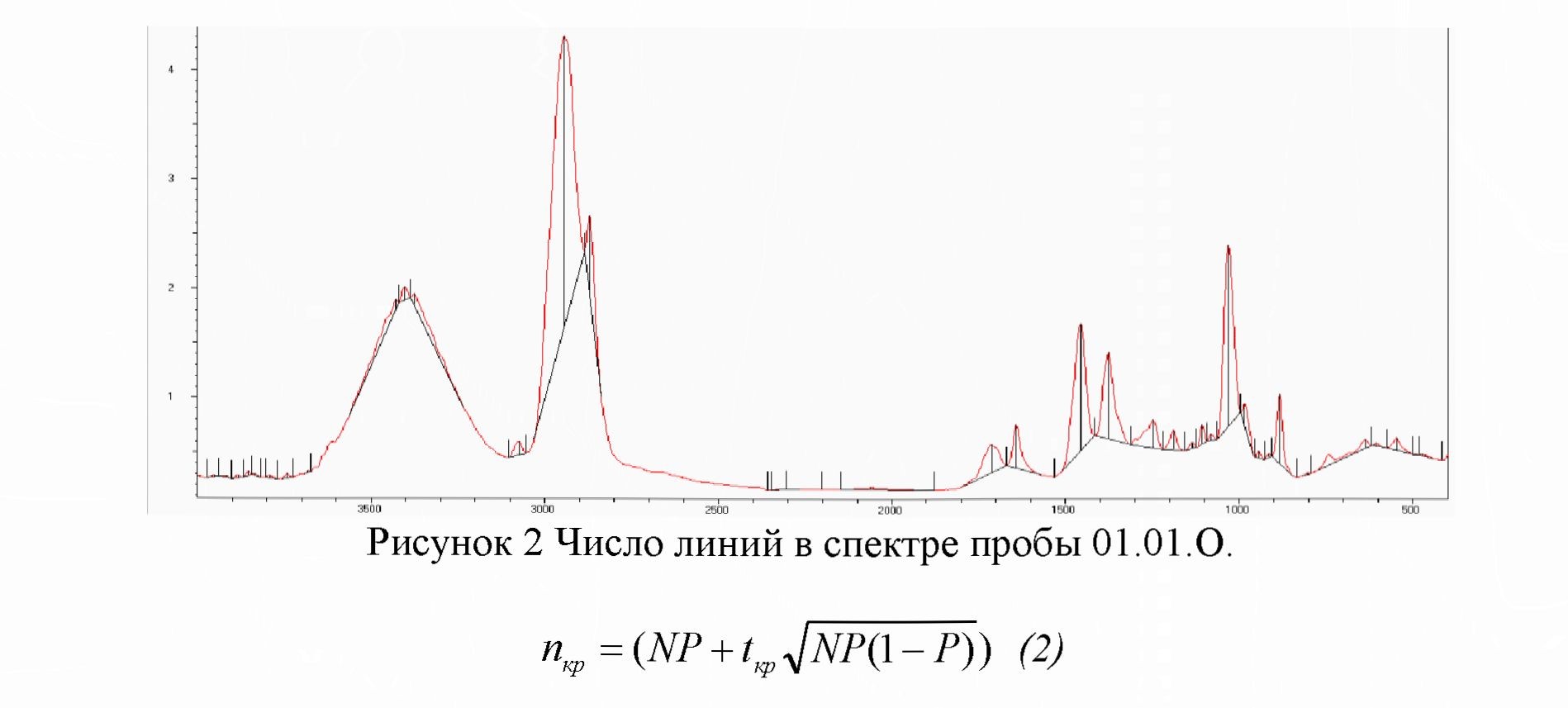
После расчета вероятности случайных совпадений линий было рассчитано максимальное число случайных совпадений-//,/, для каждой пробы по формуле 2. Число линий в ИК-спектре пробы также вычислялось с помощью программы Fspec. Например: в спектр пробы 01.01.0. количество линий А равно 25 (Рисунок 2).
N - Число линий в спектре пробы; P - вероятность проявления каждой линии в спектре пробы; tKp - табличная величина значение интеграла Гаусса равное 1,65. Число линий в ИК-спектре вычислялось программой FSpec.
Вывод о присутствии бетулина в смеси был сделан на основании сравнения значения пкр и количества найденных совпадении в спектре эталона и пробы п. Причем значение пкр всегда округляется до целочисленного значения в большую сторону. Если количество совпадений п превысит значение пкр. то мы говорим о наличии компонента. Аналогичные расчеты проводились для всех производных бетулина.
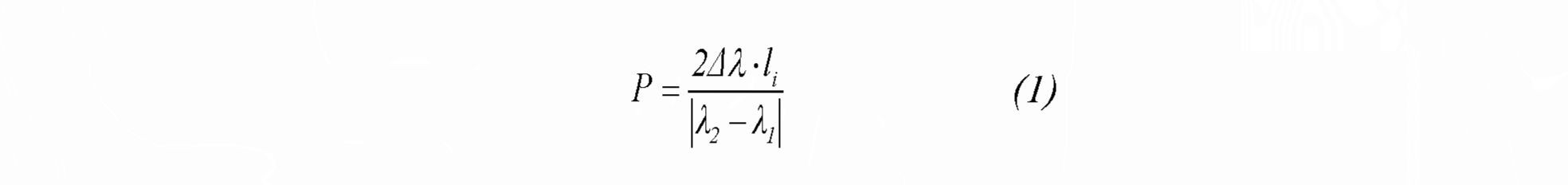
Для оценки точности и достоверности присутствия бетулина в исследуемых пробах, определенных методом ИК-спектроскопии были использованы данные, полученные методом TCX. Полученные результаты приведены в Таблице 5.
|
Исследуемая проба |
Данные ИК-спектроскопии |
Данные TCX |
|
01.01.0 |
+ |
+ |
|
02.01.0 |
+ |
+ |
|
03.01.Р |
— |
+ |
|
01.02.Р |
+ |
+ |
|
01.03.Р |
— |
+ |
|
01.04.Р |
— |
- |
Таблица 5 Сравнительный анализ присутствия бетулина в пробах,
определенногометодами ИК-спектроскопии и TCX
Анализируя полученные данные видно, что в одном случае результаты полученные методом ИК-спектроскопии не совпадают с данными полученными методом TCX. Поэтому следующим шагом стал учет статистического веса признаков. Расчет производился по формуле 3.
iJ (М+200)(Я-1)
Для расчета этой величины были использованы следующие значения: R - Число предполагаемых компонентов пробы, имеющих данный признак; M - общее число сопоставлявшихся эталонных спектров. При R = 1 величина Gy принимается равной единице.
Потом рассчитано значение пкр по формуле 2 с учетом статистического веса признаков и относительной интенсивности линий эталонных веществ. Для этого при расчете данного значения не учитывались признаки эталонных веществ, характеризующиеся небольшим статистическим весом -Gy с учетом Iomu.-
Для оценки точности и достоверности присутствия бетулина, определенного методом ИК-спектроскопии вновь проведено сравнение с данными, полученными методом TCX (Таблица 6). Можно отметить полное совпадение данных TCX и ИК-спектроскопии.
Таблица 6 Сравнительный анализ присутствия бетулина в пробах, определенного методами ИК-спектроскопии и TCX
|
Исследуемая проба |
Данные ИК-спектроскопии |
Данные тех |
|
|
Без учета статистического веса Gy |
C учетом статистического веса Gi, |
||
|
01.01.0 |
+ |
+ |
+ |
|
02.01.0 |
+ |
+ |
+ |
|
03.01.Р |
- |
+ |
+ |
|
01.02.Р |
+ |
+ |
+ |
|
01.03.Р |
- |
+ |
+ |
|
01.04.Р |
- |
- |
- |
Таким образом, введение статистического веса признаков при исследовании данных позволяет увеличить достоверность результатов, полученных методом ИК-спектроскопии.
Литература:
- Лежнева М.Ю., Щинова Т.А.. Лысаков Д.Ф.. Поляков В.В. Биологически активные вещества берёзы - источник новых высокоэффективных препаратов и биологически активных пищевых добавок// Развитие фитохимии и перспективы создания новых лекарственных препаратов. Т.2 A.: Ғылым.. 2004. - 160 с.
- Н. Д. Похило, В. А. Денисенко. В. И. Баранов. Тритерпеноиды внешней коры Betulaniaximowicziana // Химия природных соединений. - 1986. - № 5. - С. 650-652.
- В. Ф. Семенченко. Тритерпеноиды видов Betula и рода GlycyrrhizaL. Современные сведения о применении их в медицине и народном хозяйстве. M.: Наука, 1993. - С. 560.
- М. Д. Машковский. Лекарственные средства. В 2 т. - M.: ООО «Новая волна». 2001. - С. 730.
- Т. Фуджиока, И Кашивада. Р. Килкаски. Средства против СПИД. Бетулиновая кислота и платановая кислота как анти-вич факторы из Syzigiumclaviflorum. // Журнал природных продуктов. - 1994. - № 2. - С. 243-247.
- В. Dinda, I. Baneijee. S. Gulia. Triterpenes from Ajugamacrospenna Wall. // J. Indian Chem. - 1997. -№ 5. -P. 424.
- R. Ekman. The Suberin Monomers and Triterpenoids from the Oute Bark of BetulaVerrucosaElnh//HolzTorschung. 1983. Vol. 37, № 4. P.205-211
- Вершинин В.И.. Дсрендяев Б.Г., Лебедев К.С. Компьютерная идентификация органических соединений. M.: Наука, 2002. - 169 с.
- Преч Э. Определение строения органических соединений. Таблицы спектральных данных. M.: Мир. 2006. - 438 с.