В работе представлены результаты исследований биологических проб, отобранных от больных лошадей с признаками респираторного заболевания, а так же результаты выделения герпесвируса лошадей и изучения культуральных свойств выделенного вируса. Установлено, что заболевание животных в хозяйствах Т. Рыскуловского и Кордайского районов Жамбылской области вызвано герпесвирусом лошадей. Выделен эпидемиологически актуальный для территории РК изолят герпесвируса лошадей 4 серотипа. Отработаны оптимальные условия культивирования герпесвируса лошадей 4 серотипа, позволяющие нарабатывать вирусную массу для приготовления диагностических и профилактических препаратов.
Введение
К одним из широко распространенных вирусных заболеваний относятся герпесвирусные инфекции лошадей. В настоящее время известны герпесвирусы лошадей 9 типов, представленные альфа – и гаммагерпевирусами. Из герпесвирусных болезней лошадей наибольшее экономическое значение имеют инфекции, возбудителями которых являются ВГЛ-1, вызывающий массовые аборты у кобыл, патологию органов дыхания у жеребят, спорадические случаи миелоэнцефалопатии у лошадей, независимо от возраста и физиологических особенностей; ВГЛ-4 – возбудитель ринопневмонии и спорадических абортов; ВГЛ-3 – возбудитель коитальной экзантемы лошадей, острого контагиозного заболевания, при котором поражается эпителий влагалища у кобыл и полового члена у жеребцов; ВГЛ-9 – возбудитель миелоэнцефалопатии лошадей и других гетерогенных хозяев: газелей, зебр, антилоп - часто с летальным исходом. Вирусы 2 и 5 типов (гаммагерпесвирусы) вызывают латентную инфекцию, а также участвуют в развитии респираторных поражений у жеребят. Наиболее значимые для коневодства заболевания вызывают вирусы 1-го (вирусный аборт) и 4-го (ринопневмония) типов [1, 2].
Ринопневмония - это вирусная инфекция лошадей, которая может проявляться поражением органов дыхания, абортами, пневмонией новорожденных жеребят или миелоэнцефалитами. Ранее заболевание было описано разными названиями: вирусный аборт кобыл, половая экзантема лошадей, катаральная инфлюэнца, герпес, ринотрахеит лошадей [1-3].
В естественных условиях болеют лошади, пони, ослы и мулы всех возрастов и пород независимо от пола. Более чувствительны чистокровные породы и молодняк до 1 года.
Различные штаммы вируса ринопневмонии размножаются в первичных культурах и субкультурах почек лошадей, пони, свиньи, теленка, овцы, тестикуллов, легких и селезенки лошади, а также в перевиваемых линиях клеток BHK-21, AND, HeLa, RK-13. Размножение вируса в чувствительных культурах клеток сопровождается развитием цитопатических изменений характерных для вирусов группы герпес. Штаммы вируса, адаптированные к культурам клеток, оказывают более выраженный цитопатический эффект и накапливаются в высоких титрах. Цитопатогенное действие адаптированных штаммов наступает через 24-48 часов, а неадаптированных через 3-5 суток. Первым признаком цитопатических изменений служит появление отдельных округленных светлых клеток через 24-36 часов после заражение. В менее чувствительной к вирусу перевиваемой линии клеток почки теленка цитопатическое изменения в первые 2-3 суток имеют очаговый характер, затем они постепенно распространяются по всему монослою клеток. Пораженные клетки округляются и отделяются от стекла, в них образуются внутриядерные эозинофильные тельца-включения [4].
Ранее нами было показано, что ГПЛ 1 и 4 серотипов циркулируют в популяциях лошадей в различных регионах РК [5, 6].
Целью настоящей работы было определение эпизоотической ситуации по герпесвируса лошадей в различных регионах РК, выделение эпидемиологически актуального штамма герпесвируса лошадей циркулирующего на территории РК и изучение культуральных свойств выделенного вируса.
Материалы и методы
Материалом для исследования служили 114 проб (из них 105 смыва, 9 патологических материалов) от лошадей разных регионов Казахстана.
При постановке ПЦР в качестве положительного контроля использовали ДНК вакцинного штамма СВ/69.
Выделение ДНК из образцов проводили с помощью набора «Viral DNA Mini Kit»,
фирмы «Qiagen», в соответствии с инструкцией производителя.
Для выявления ГВЛ лошадей использовали праймеры специфические на ГВЛ 1- серотипа BS-1-P1и gB1-R-2 (1-раунд), BS-1-P3 и gB1-R-a (2-раунд), а также праймеры специфические на ГВЛ 4-серотипа BS-4-P1 BS-4-P2 (1-раунд), BS-4-P3 и BS-4-P4 (2- раунд) [5].
ПЦР проводили с помощью коммерческого набора фирмы «Invitrogen».
Реакционная смесь для постановки реакции состояла из следующих компонентов: вода - 31,5 мкл; 10хбуфер - 5 мкл; dNTPS - 1 мкл; R праймер - 5 мкл; F праймер - 5 мкл; MgCl2 - 2,5 мкл; TaqDNA polymerase - 0,5 мкл; ДНК - 2 мкл.
Постановку ОТ-ПЦР проводили при следующем температурном режиме: преденатурация – 94 °С - 4 мин; денатурация – 94 °С – 30 сек; отжиг - 60 °С - 30 сек; репликация – 72 °С – 90 сек, пост-репликация – 72 °C – 10 мин.
Амплификацию проводили на приборе «MasterCycler» фирмы «Eppendorf», в течение 40 циклов.
Электрофоретическое разделение продуктов амплификации проводили в 1,5 % агарозном геле в присутствии бромистого этидия.
Анализ продуктов амплификации проводили в 1,5 % агарозном геле на TAE
буфере. Размер ампликона на 1серотип - 770 п.о., на 4 серотип - 580 п.о.
Электронную микроскопию проводили методом негативного контрастирования с использованием 4 % раствора фосфорно-вольфрамовой кислоты с рН 6.8. Вирус из органо-тканевого материала выделяли методом ультрацентрифугирования при 35000 об/мин в течение 45 мин из осветленного гомогената. Адсорбцию вируса на сетки с фарфоровой подложкой напыленной углеродом проводили на капле вируссодержащей жидкости в лунке тефлоновой пластины. Время адсорбции составляло 10 мин. После адсорбции сетку с образцом контрастировали на капле фосфорно-вольфрамовой кислоты в течение 5 мин и после просушивания исследовали в электронном микроскопе JEM-100 CX II JEOL при ускоряющем напряжении 80 Kv и увеличении 20-40 тысяч.
Культуры клеток выращивали в среде Игла МЕМ с добавлением 2 мМ глутамина, 5 % сыворотки крови КРС для культур клеток, пенициллина по 100 ЕД/мл и стрептомицина по 100 мкг/мл.
Для выделения вируса использовали однодневную диплоидную клеточную культуру почки кролика (RK-13). Для этого с пробирок (матрасов) со сплошным клеточным монослоем сливали ростовую питательную среду, клетки 1 - 2 раза промывали раствором Хенкса для удаления сывороточных антител и ингибиторов. В каждую пробирку (матрас) вносили соответствующее количество вируссодержащего материала и с помощью покачивания распределяли его равномерно по слою клеток и для адсорбции вируса оставляли в течение 1 - 2 часа при комнатной температуре. После этого вируссодержащий материал удаляли и добавляли поддерживающую среду (в пробирку 1 - 2 мл, в матрасы около 10% объёма). Инкубировали в термостате при 37 оС. Все пробирки (матрасы) после заражения клеток ежедневно исследовали под малым увеличением микроскопа на наличие цитопатического действия (ЦПД), сравнивая культуры клеток, заражённые вирусом, с контрольными. Титр вируса определяли по инфекционному действию на культуру клеток и оценивали по методу Рида и Менча [7].
Результаты и обсуждение
С целью выяснения эпизоотической ситуации в РК по ринопневмонии лошадей в 2011-2012 гг. нами был проведено обследование хозяйств Жамбылской, Южно- Казахстанской, Алматинской, Костанайской, Северо-Казахстанской областей и собрано 114 проб патологического материала от абортированных плодов лошадей и носоглоточных смывов.
Исследование проб, доставленных из различных регионов РК, на наличие вируса ринопневмонии проводили методом ОТ-ПЦР и электронной микроскопии. Результаты исследования биологических проб в ПЦР представлены в таблице 1.
Таблица 1 - Результаты ОТ-ПЦР на ГВЛ
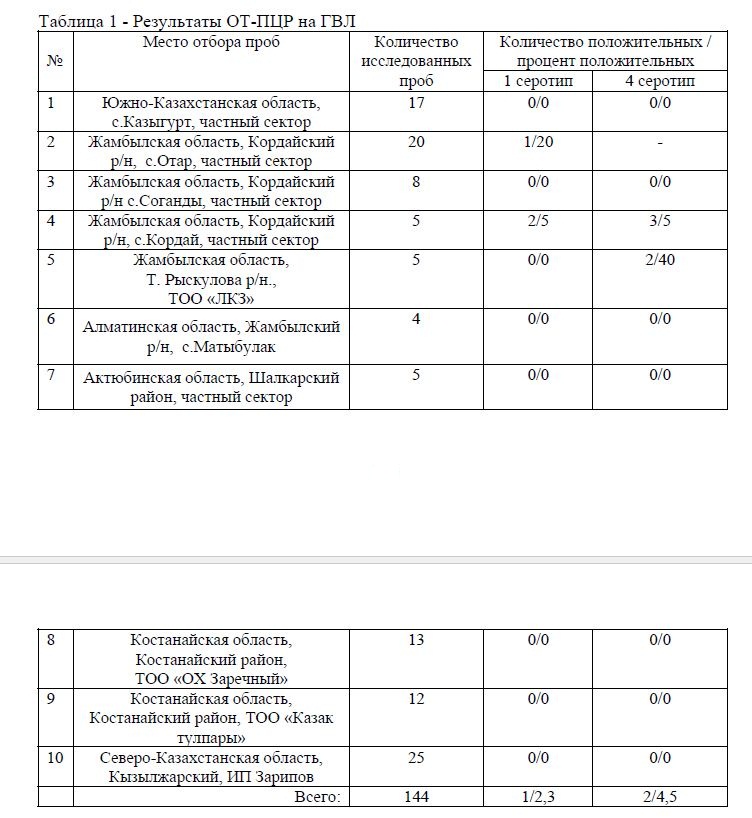
В результате проведенных исследований установлено, что в 1 пробе из 5 доставленных из с. Отар Кордайского района Жамбылской области выявлен ГВЛ серотипа 1, в двух пробах из 5 доставленных из ТОО ЛКЗ Т.Рыскуловского района Жамбылской области выявлен ГВЛ серотипа 4, в пробах доставленных из п.Кордай Кордайского района Жамбылской области выявлен ГВЛ обоих серотипов.
Для выделения вирусов использовали диплоидную клеточную культуру почки кролика RK-13. Материалом для выделения вируса служили 20 % суспензии из паренхиматозных органов (легких, печени, селезенки), содержимое желудка плода и смывы из носовой полости.
В результате проведенных исследований на первом пассажном уровне из материала, доставленного из Т.Рыскуловского района Жамбылской области, был выделен цитопатогенный агент. Специфическое цитопатогенное действие наступало через 24-36 часов, первым признаком цитопатических изменений служило появление отдельных округленных, светлых клеток через 36 часов после заражения, затем они постепенно распространялись на весь клеточный пласт.
ПЦР исследование выделенного возбудителя позволило идентифицировать ГВЛ 4 серотипа.
В результате электронномикроскопических исследований в культуральных пробах был обнаружен вирус, который по морфологии и размерам вириона характерно к ГВЛ. Вирион имеет суперкапсид (наружную оболочку) диаметром 200-210 нм и центральный капсид гексогональной формы диаметром 80-90 нм (рисунок 1).
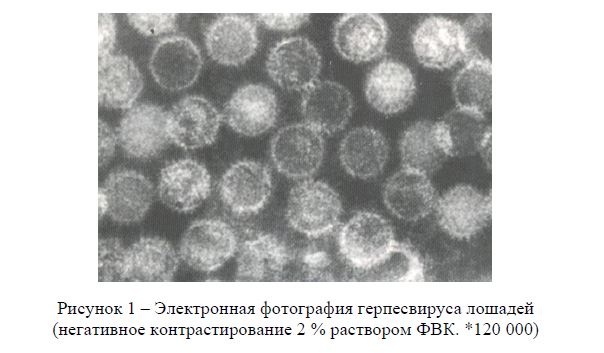
Рисунок 1 – Электронная фотография герпесвируса лошадей (негативное контрастирование 2 % раствором ФВК. *120 000)
С целью изучения культуральных свойств выделенного возбудителя было проведено 3-7 последовательных пассажей с использованием 1-2 суточной культуры клеток Vero, RK-13, BHK-21, СПЭВ, ПТ-80.
Культивирование проводили в стационарных условиях в матрасах и пробирках в течение 2-10 суток при 37 оС до 70-90 % поражения монослоя клеток. Полученные пробы вируссодержащего материала каждого пассажного титровали в одноименной культуре клеток с целью определения биологической активности.
Результаты исследований по определению чувствительности различных культур клеток к вирусу ГПЛ представлены в таблице 2.
Таблица 2 – Чувствительность различных культур клеток к вирусу ринопневмонии лошадей
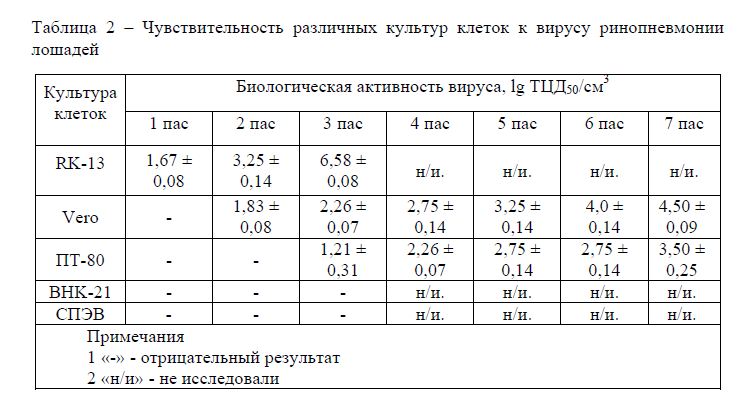
В результате проведенных исследований было установлено, что наиболее активные вирусные материалы получены в культуре клеток RK-13, на уровне 3-го пассажа титр вируса составлял 6,58 ± 0,08 lg ТЦД50/см3. Цитопатическое действие вируса проявлялось на 1-2 сутки.
Менее чувствительными культурами клеток оказались ПТ-80 и Vero, титр на уровне 7-го пассажа вируса составлял 3,50 ± 0,25 и 4,50 ± 0,09 ТЦД50/см3, соответственно. ЦПД не было отмечено в перевиваемых культурах клеток BHK-21 и СПЭВ.
В дальнейших исследованиях использовали перевиваемую линию культуры клеток RK-13.
Отработка оптимальных условий культивирования показало, максимальное накопление вируса ГВЛ 4 серотипа в культуре клеток при заражающей дозе от 0,01 до 1,0 ТЦД50/см3 с инкубированием при 37 оС в течение 2-3 суток обеспечивает получение вируса с биологической активностью до 6,58 ± 0,08 lg ТЦД50/см3.
Выводы
Таким образом, результаты проведенных исследований показали, что ГВЛ обоих серотипов циркулирует среди конепоголовья Жамбылской области. В культуре клеток RK-13 выделен изолят ГВЛ 4 серотипа. Отработаны оптимальные условия культивирования ГВЛ 4 серотипа, позволяющие нарабатывать вируссодержащую суспензию пригодную для приготовления диагностических и профилактических препаратов.
Литература
- Юров К.П. Инфекционные болезни лошадей // Изд-во «Грааль». – 2000. – С.19 -36.
- OIE - World organization for animal health / World Animal Health Information Database (WAHID) Interface //http://www.oie.int/wahis_2/public/wahid.php/ Countryinformation / Countryre ports
- Patel J.R., Heldens J. Equine herpesviruses 1 (EHV-1) and 4 (EHV-4)-epidemiology, disease and immunoprophylaxis: a brief review // Vet J. – 2005. – Vol. 170, № – P. 14-23.
- Татаурова А. В., Юров К. П., Алексеенкова С. В. Нейропатогенные штаммы возбудителя ринопневмонии – вирусного аборта лошадей. // Ветеринария, 3,– 23.– С.20
- Омарова З., Керимбаев А., Мусаева Г., Орынбаев М.Б. Обнаружение и типирование герпесвируса лошадей методом ПЦР // Сборник материалов международной научно-практической конференции молодых ученых, посвященной 55- летию НИИПББ. Гвардейск-2013г. С.152-159
- Шалгынбаев Э., Рябинникова А., Рыстаева Р., Омарова З., Орынбаев М.Б. Выделение и культивирование вируса ринопневмонии лошадей на культуре клеток // Материалы 2-ой международной научно-практической конференции молодых ученых, посвященный дню образования НИИПББ. Гвардейск, август, 2014 г. С.196-200
- Reed J. A simple method of estimating fifty per cent endpoints // Am. J. Hyd. – 1938. –Vol.27. – P. 493-497.