В статье приведены данные о результатах исследования биологических свойств листерий, выделенных от овец. Определение биологических свойств, культивирование листерий, определение ферментативных свойств листерий. Выделенная культура листерий имеет характерные биологические свойства и высокую вирулентность. Выделенная культура листерий обладает устойчивостью к стрептомицину, метициллину, неомицину.
Введение Листериоз регистрируют почти в 60 странах мира. Экономический ущерб определяется высокой летальностью, снижением продуктивности животных, затратами на лечебно-профилактические и карантинно-ограничительные мероприятия [1].
Листериоз–природно-очаговая, зооантропанозная болезнь, характеризующаяся полиморфизмом клинических проявлений и синантропностью. Листериоз является одной из широко распространенных бактериальных инфекций в Казахстане и представляет актуальную проблему. К листериозу восприимчивы все виды домашнихживотных: овцы, козы, крупный рогатый скот, свиньи, лошади, кролики, морские свинки, птицы, а также люди. Механизм заражения людей многообразен, чаще всего происходит алиментарным путем через инфицированную воду и пищевые продукты животного происхождения, особенно, при отсутствии надежной термической обработки и длительном хранении в условиях относительно низких температур [2].
Возбудитель листериоза–Listeria monocytogenes. Источник возбудителя инфекции - больные и переболевшие животные (листерионосители). В проявлении и распространении листериоза отмечена большая роль резистентности организма животного и условий внешней среды [3].
Листерии долго сохраняют свою жизнеспособность и, в отличие от других микроорганизмов, обладают способностью размножаться при температуре 400С. В почве, навозе возбудитель сохраняет жизнеспособность до 11-12 месяцев, в сене – до 20, в трупе – до 4, в прудовой воде до 1 года.
Выделяют четыре клинические формы листериоза: нервная, ангинозно-септическая, глазо-железистая и тифоидная. При нервной форме листериоза происходит абсцесс мозга, менингит и энцефалит. Эти заболевания могут стать причиной паралича и различных психических расстройств. Чаще всего у людей встречается ангинозно-септическая форма листериоза, которая проявляется в виде ангины с тифоподобным течением и нервным синдромом. При этой форме листериоза у больного наблюдается увеличение миндалин и лимфатических узлов, покраснение горла и незначительное повышение температуры.
Диагностируют листериоз на основании лабораторных исследований, при этом очень важно проводить дифференциальную диагностику болезни, чтобы отличить каждую форму болезни от заболевания со схожими симптомами. Например, для отличия тифоидной формы листериоза от брюшного тифа или псевдотуберкулеза [4].
Цель исследования – проведение бактериологического исследования патологического материала от павших овец и абортированных плодов и идентификация листерий по биологическим свойствам.
Материалы и методы исследования Исследования проводились в лаборатории противобактериозной биотехнологии кафедры “Биологическая безопасность” Казахского национального аграрного университета. Объектом исследования были абортированный плод и внутренние органы павших овец. Материал был доставлен из хозяйств Алматинской области. По клиническим признакам и патолого-анатомическим исследованиямбыл поставлен предварительный диагноз - листериоз. Нашей задачей являлось выделение культур листерий и их идентификация.
Микроскопическое исследование проводили после окрашивания препаратов по методу Грама. Подвижность листерий определяли в суточной культуре приготовлением препарата «висячая капля».
Для определения культурально-морфологических свойств были использованы следующие среды: МПА, МПБ с добавлением 1% глюкозы и 2% глицерина и картофельный агар.
Для повышения высеваемости листерий применили метод Грея, при котором учитывается способность листерий размножаться длительное время в мертвых тканях. В кусочки органов добавили полимиксин и поместили в холодильник на 5 дней. Затем сделали посев на МПА и МПБ.
Биохимические свойства листерий изучали путем проведения посевов на среды Гисса. Учет результатов проводили следующим образом: после посева бактерий, если они ферментируют углеводы, наблюдают появление красной расцветки, которая свидетельствует об изменении рН в кислую сторону (образование кислоты), порой из поплавка вытесняется жидкость. В этом случае делали вывод об образовании газа. Для определения каталазной активности делали посев на поверхность плотной питательной среды. Затем наносили каплю 10%-го раствора Н2О3 на выросшую колонию. Выделение О2, хорошо заметное по образованию пузырьков, свидетельствует о наличии в клетках каталазы.
Протеолитические свойства определяли посевом на желатину.
Патогенность определяли, заразив белых мышей чистой культурой бактерий, и наблюдали за изменениями. Для постановки биопробы взяли по 3 белой мыши на 1 штамм.
Для определения чувствительности к антибиотикам применили чашечный метод с использованием бумажных дисков, пропитанных растворами различных концентраций испытуемого антибиотика. Исследуемую культуру смыли с агара физиологическим раствором, приготовили взвесь 1012 КОЕ и 1 см3 ее засеяли сплошным слоем по всей поверхности агара. Засеянные чашки подсушили в термостате 30 мин при 370С. Бумажные диски с антибиотиками разложили на засеянный агар стерильным пинцетом на расстоянии 2см от края, слегка прижимая к среде. Учет результатов производили по величине зоны задержки роста микробов вокруг бумажных дисков, включая их диаметр[5].
Результаты исследований их обсуждение Изучаемая культуралистерий на МПА росла на чашках с агаром в виде мелких, слизистых, круглых, прозрачных колоний, при проходящем или молочно-белых в падающем свете, выпуклы колонийдиаметром 0,2- 0,4 мм. Через 3-4дня колонии увеличивались в диаметре до 3 мм, приобретали серовато – белый цвет и неровные расплывчатые края.
На МПБ отмечались помутнения с образованием слизистого осадка. Для дифференциации листерий от пастерелл был использован картофельный агар с добавлением 1% глюкозы и 2% глицерина. При этом тестируемая культура выросла. Как известно, пастереллы на этих средах не растут.
Выделенные листерии были подвижны при температуре от 220С до 370С. В мазках из образовавшихся колоний, окрашенных по граму, листерии располагались параллельно друг к другу, одиночно или в коротких цепочках, или V-образно, окрашенные в фиолетовый цвет (Рисунок 1).
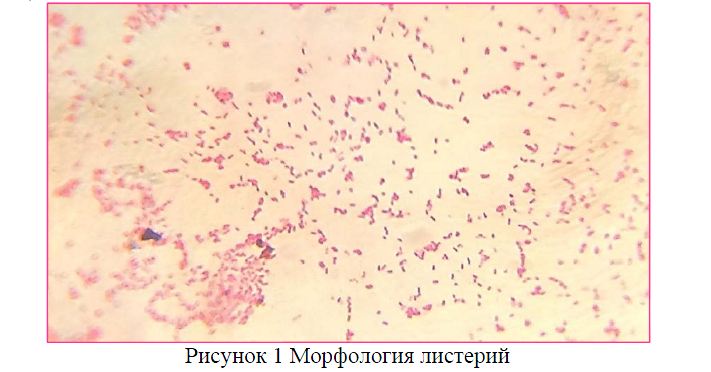
Рисунок 1 Морфология листерий
Для дальнейшей идентификации нами проведено исследование ферментативной активности тестируемой ультуры. Результаты исследования отражены в таблице 1.
Таблица 1- Биохимические свойства выделенных листерий
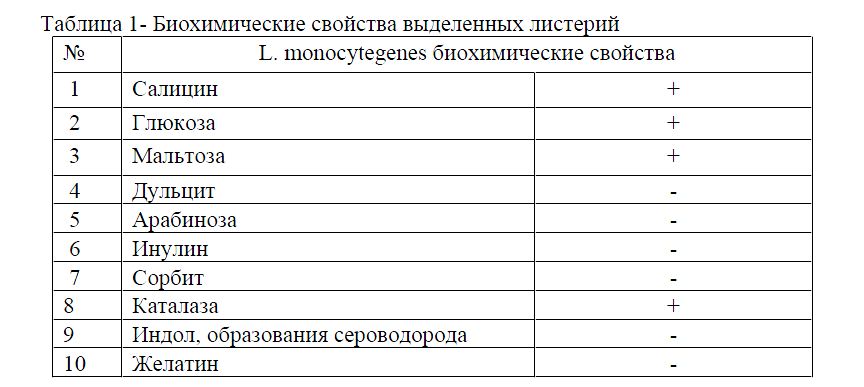
Как видно из таблицы 1, культура листерий обладает сахаролитическими свойствами. Листерии ферментируют глюкозу, мальтозу, салицин, но не ферментируют арабинозу, дульцит, инулин, сорбит. Обладают каталазной активностью, не выделяют уреазу, не образуют индол, продуцируют ацетил – метил – карбинол. Сероводород и индол на обычных средах не образует.
Желатин листерии не разжижают. Через 10 -12 суток в желатине образовался рост изучаемых штаммов листерий в виде мелких гранул.
Для изучения вирулентных свойств листерий нами была поставлена биопроба на белых мышах. Предварительно проведена титрация смыва с агаровой культуры до концентрации 107 КОЕ. Для каждой дозы культуры использовали по 3 мыши. Результаты представлены в таблице 2.
Таблица 2 - Определение патогенности культур
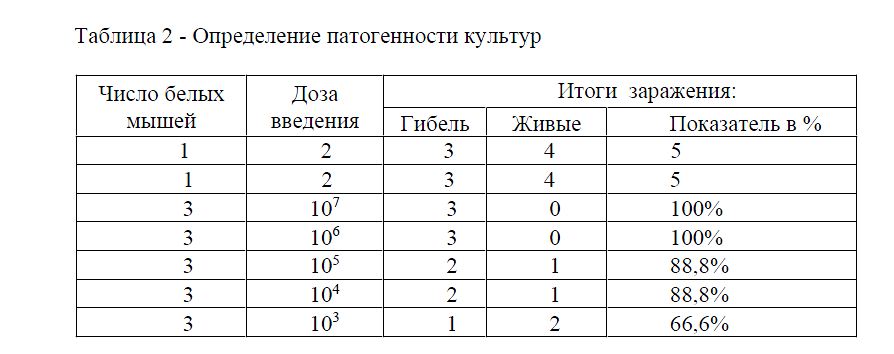
Гибель животных начала отмечаться с 3 суток. При вскрытии лабораторных животных отмечались идентичные патологоанатомические изменения, которые проявлялись увеличением печени и селезенки с характерными серо – белыми очагами на органах.
При этом установлено, что доза 106-107 КОЕ вызывает гибель 100% лабораторных животных. Даже доза 103 КОЕ привела к гибели 66,6% взятых в опыт животных. Это свидетельствует о высокой вирулентности изучаемой культуры.
По морфологическим, культуральным, биохимическим свойствам и патогенности выделенная культура нами была идентифицирована как Listeria monocytogenes.
Важным этапом бактериологического исследования является определение чувствительности штаммов к антибиотикам. По литературным данным, если зона задержки роста составляет 15 - 25 мм, то считают, что микробы чувствительны к антибиотику, до 15 мм — малочувствительны; отсутствие такой зоны указывает на резистентность бактериальной культуры к данному антибиотику. Результаты изучения чувствительности к антибиотикам представлены в таблице 3.
Таблица 3 - Чувствительность листерий к антибиотикам
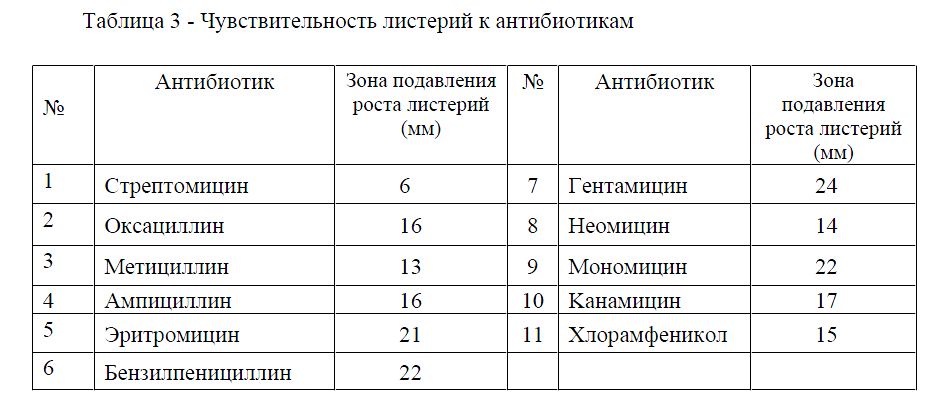
Как видно из таблицы 3, выделенные культуры листерий показали высокую чувствительность к бензилпенициллину, эритромицину, гентамицину и мономицину, но оказались малочувствительны к стрептомицину, метициллину, неомицину.
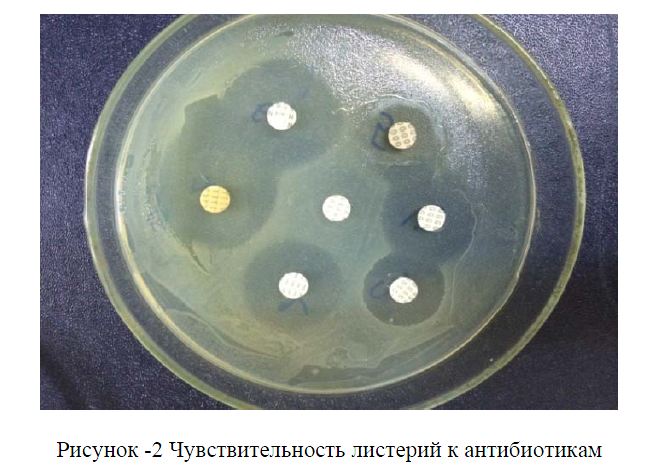
Рисунок -2 Чувствительность листерий к антибиотикам
Выводы
- Листериоз овец регистрируется в хозяйствах Алматинской области, нанося экономический ущерб и представляя опасность для людей.
- Выделеная нами культура листерий имеют характерные биологические свойства и высокую вирулентность.
- Выделенная культура листерий обладает устойчивостью к стрептомицину, метициллину, неомицину, но чувствительна к бензилпенициллину, эритромицину, гентамицину и мономицину.
Исходя из всего материала нельзя недооценивать всю опасность листериоза. В обязательном порядке нужно проводить специфическую профилактику листериоза, организовывать ветеринарно-гигиенические мероприятия в населенных пунктах, в животноводческих хозяйствах и предприятиях по переработке продуктов животного происхождения.
Литература
- Инфекционные болезни животных / Бессарабов Б.Ф. , Воронин Е.С. и др.; Под ред. А.А. Сидорчука. – М.: КолосС, 2007. – 671 с
- Киркимбаева Ж.С. Частная микробиология. - Алматы, 2009 – 271 с.
- Радчук Н.А, Дунаев Г.В. Ветеринарная микробиология и иммунология / Радчук Н.А, Дунаев Г.В.-М.: Агропромиздат,1991.-С.202-205.
- Середа Д.А., Котлярова В.М. Иммунитет при листериозе «Журнал микробиологии, эпидемиологии, иммунологии».- №5.- С. 98-102.
- Кисленко В.Н. Практикум по ветеринарной микробиологии и иммунологии. Москва, 2005 - 232 с.