В статье изучены некоторые аспекты биохимии, в частности, определение in vitro активности пере-кисного окисления липидов и ферментативной системы антиоксидантной защиты нейтрофилов и моноцитов крови человека. Было проведено исследование крови, поскольку кровь является важным диагностическим методом при различных патологических состояниях организма. В ходе изучения показателей перекисного окисления липидов и системы антиоксидантной защиты на культурах нейтрофи-лов и моноцитов, выделенных из периферической крови у лиц мужского пола, было установлено, что взаимодействие in vitro липосахаридов бактерий рода Shigella с субпопуляциями Т-лимфоцитов вызывает изменение как активности перекисного окисления липидов, так и активности ферментативной системы антиоксидантной защиты.
Введение
Перекисное окисление липидов (ПОЛ) играет важную роль в жизнедеятельности любой клетки, влияя как на состояние всех её мембранных структур, так и на функциональную активность клеточных органелл, и прежде всего митохондрий [1, 2]. Активность ПОЛ регулируется системой антиок-сидантной защиты (АОЗ), ключевыми энзимами которой являются каталаза и супероксиддисмутаза (СОД) [3, 4]. Усиление ПОЛ при недостаточности системы АОЗ способно запустить в клетке программу апоптоза, в частности, через митохондриальный путь [2]. Активацию ПОЛ способны вызвать гипоксия и токсические субстанции, к числу последних относятся и структурные компоненты клеточных стенок грамнегативных бактерий — липополисахариды (ЛПС) [1, 2]. Нарушение баланса в системе ПОЛ/АОЗ в субпопуляциях иммунорегуляторных Т-лимфоцитов, вероятно, обусловливает развитие иммунодефицитного состояния, в том числе и при таком инфекционном заболевании, как шигеллёз, возбудителями которого являются грамнегативные виды бактерий из рода Shigella.
Влияние шигеллёзных ЛПС на ПОЛ и ферментативную систему АОЗ Т-лимфоцитов крови человека in vitro до настоящего времени не исследовалось. Работа является фрагментом плановой научной темы кафедры микробиологии ГУ «Луганский государственный медицинский университет» № 01110U007081 «Иммуносупрессивный и апоптогенный потенциал условно-патогенных бактерий и грибов».
Целью настоящего исследования явилось определение in vitro активности ПОЛ и ферментативной системы АОЗ нейтрофилов и моноцитов крови человека под воздействием ЛПС бактерий рода Shigella.
Материалы и методы исследования
Изучение показателей ПОЛ и системы АОЗ проводилось на культурах нейтрофилов и моноцитов, выделенных из периферической крови 48 практически здоровых лиц мужского пола 19-24 лет (средний возраст — 22,4±1,3 года). Работу выполняли с соблюдением всех положений биоэтики (Страсбург, 1985 г.).
Лимфоциты выделяли на градиенте плотности фиколла-верографина (р = 1,076) по модифицированной методике Boyum [5]. Сепарацию Т-лимфоцитов от популяций НК-лимфоцитов и В-лимфо-цитов, моноцитов и нейтрофилов осуществляли с помощью моноклональных антител CD14, CD16 и СD22 (производства НПЦ «Медбиоспектр», Москва, РФ). Для этого в суспензию лимфоцитов вносили указанные антитела в разведении 0,1-0,2 мкг/мл в количестве 0,025 мл с последующим через 40 мин добавлением комплемента морской свинки, разведенного изотоническим раствором натрия хлорида в соотношении 1:1. Смесь инкубировали 60 мин в термостате, после чего Т-лимфоциты трижды отмывали при центрифугировании в среде 199. Сепарацию Т-лимфоцитов на субпопуляции Т-хелперов/индукторов и Т-супрессоров/цитотоксиков осуществляли при помощи моноклональных антител CD4 и CD8 по аналогичной методике. Рабочая концентрация суспензий Т-лимфоцитов составляла 2*(9 lg)A
ЛПС получали из культур Shigella flexneri (серовары 1a, 1b, 2a, 2b) и Shigella sonnei по методу [6, 7]. Идентификацию шигелл проводили с использованием диагностических наборов «Энтеро-тест 24» производства фирмы Микро-ЛА-Тест, АО «Лахема», Чехия. Идентификацию сероваров Sh. flexneri проводили в реакции агглютинации с шигеллёзными О-сыворотками. Для стимуляции in vitro нейтрофилов и моноцитов использовались ЛПС в концентрациях 1-10-100 мкг/мл.
Перед определением внутриклеточного содержания диеновых конъюгатов (ДК) и малонового диальдегида (МДА), активности каталазы и супероксиддисмутазы (СОД) клеточные культуры ней-трофилов и моноцитов лизировали стерильной бидистиллированной водой в течение 15 мин при комнатной температуре. Определение ДК осуществляли по методу И.Д.Стальной (1977) [4], определение МДА — по методу И.Д.Стальной и Т.Г.Гаришвили (1977) [8]. Активность каталазы изучали по М. А. Королюк и соавт. (1988) [3], активность СОД — спектрофотометрическим методом [9]. О балансе в системе ПОЛ/АОЗ судили по интегральному коэффициенту К (у.е.), который высчитывали по формуле К = (ДК + МДА)/(каталаза + СОД). Статистическая обработка полученных данных проводилась с использованием критерия Стью-дента.
Результаты исследования и их обсуждение
В результате проведенного исследования было установлено, что взаимодействие in vitro шигел-лёзных ЛПС с субпопуляциями Т-лимфоцитов вызывает изменение как активности ПОЛ, так и активности ферментативной системы АОЗ. При этом степень выраженности указанного влияния зависела от действующей концентрации шигеллёзных ЛПС и продолжительности их контакта с клетками-мишенями и не зависела от видовой и антигенной принадлежности использованных ЛПС. Результаты проведенного исследования представлены в таблицах 1 и 2.
Как оказалось, непосредственный контакт in vitro шигеллёзных ЛПС с CD4+- и CD8+-лимфо-цитами (Т-хелперы/индукторы и Т-супрессоры/цитотоксики, соответственно) вызывал в указанных клетках увеличение внутриклеточного содержания и промежуточных (ДК), и конечных (МДА) продуктов ПОЛ, уровни которых возрастали по мере увеличения продолжительности контакта ЛПС с иммуноцитами. Наиболее высокие концентрации изучаемых метаболитов ПОЛ регистрировались на 24-м часу эксперимента, независимо от действующей концентрации использованных ЛПС. Однако активация ПОЛ под влиянием ЛПС в дозе 100 мкг/мл значительно превосходила таковую при использовании шигеллёзных ЛПС в дозе 10 мкг/мл. Так, в частности под воздействием ЛПС Shigella sonnei (10 мкг/мл) на 24-м часу опыта внутриклеточная концентрация ДК в культурах CD4+-лим-фоцитов была в 1,46 раза ниже таковой в опытах с Shigella sonnei (100 мкг/мл), а концентрация МДА — ниже в 2,14 раза (р < 0,05 в обоих сравнениях). Сходные различия имели место и при использовании ЛПС Shigella flexneri 1а и Shigella flexneri 1b.
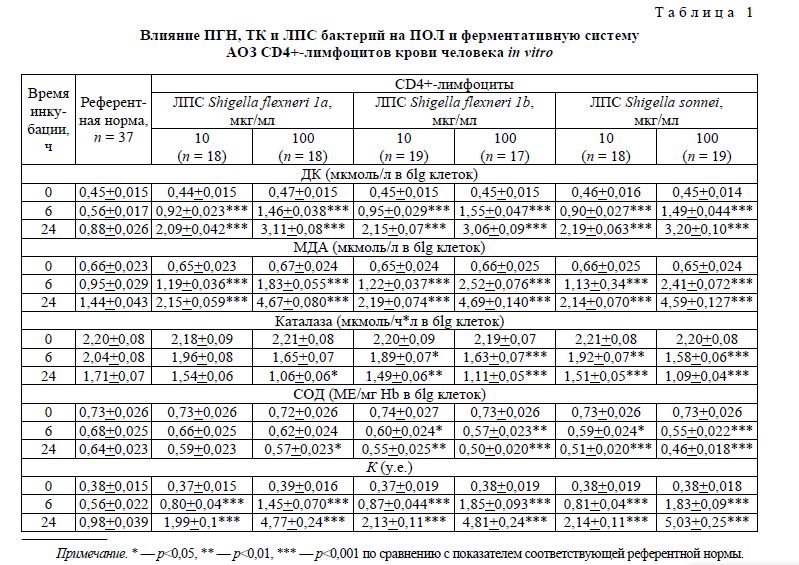
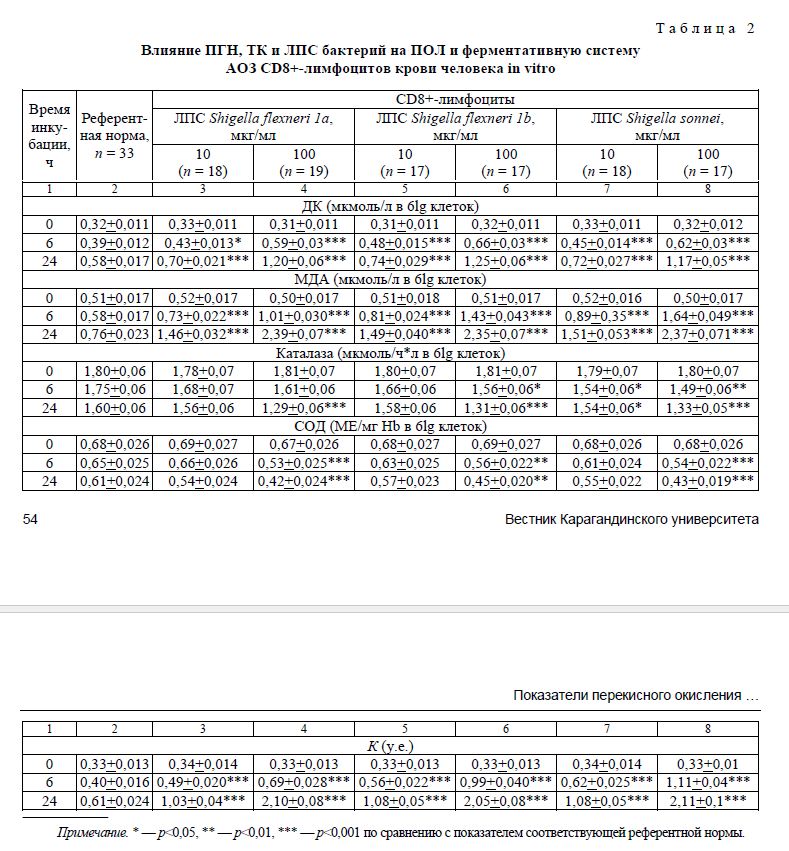
Активность каталазы и СОД в CD4+-лимфоцитов и в CD8+-лимфоцитах с увеличением длительности их контакта с шигеллёзными ЛПС, а также с увеличением действующей концентрации последних, напротив, снижалась. Нарушения в ферментативной системе изучаемых субпопуляций Т-лимфо-цитов были наибольшими на 24-м часу эксперимента, при воздействии на Т-клетки шигеллёзных ЛПС в действующей концентрации 100 мкг/мл.
Так, в субпопуляции CD8+-лимфоцитов, находившихся в контакте с ЛПС Shigella flexneri la указанной дозы, активность каталазы и СОД на 24-м часу исследования оказалась в 1,24 и 1,45 раза ниже референтной нормы, соответственно (р<0,01). В то же время показатели активности каталазы и СОД, зарегистрированные также на 24-м часу опытов, но с ЛПС Shigella flexneri la в дозе 10 мкг/мл, были ниже референтной нормы соответственно в 1,02 и 1,13 раза (р>0,05 в обоих сопоставлениях).
Указанные разнонаправленные сдвиги показателей ПОЛ и ферментативной системы АОЗ в субпопуляциях CD4+- и CD8+-лимфоцитов сопровождались увеличением коэффициента К, характеризующего баланс в системе ПОЛ/АОЗ, что свидетельствовало о преобладании процессов ПОЛ над активностью ферментативной системы АОЗ. Наибольшие негативные изменения коэффициента К имели место при использовании шигеллёзных ЛПС в действующей концентрации 100 мкг/ мл и экспозиции с клетками-мишенями 24 ч.
При проведении сравнительного анализа видоспецифического влияния шигеллёзных ЛПС на субпопуляции Т-лимфоцитов выявлено не было.
Выводы
ЛПС бактерий рода Shigella (Shigella flexneri, Shigella zonnei) оказывают in vitro дозозависимое и видонеспецифическое влияние на активность ПОЛ и ферментативной системы АОЗ нейтрофилов и моноцитов крови человека. Наиболее выраженную активацию ПОЛ и недостаточность ферментативной системы АОЗ инициируют шигеллёзные ЛПС в действующей концентрации 100 мкг/мл, умеренные изменения — ЛПС в дозе 10 мкг/мл. Шигеллёзные ЛПС в действующей концентрации 1 мкг/мл негативного влияния на ПОЛ и ферментативную систему нейтрофилов и моноцитов крови человека in vitro не оказывают.
Список литературы
- Шабельник О.І., Гайдаш І.С., Флегонтова В.В. Впливinvitroрізних методів інактиваціі токсинів сальмонелл на метаболічний статус моноцитів, нейтрофілів та ентероцитів. — Львів: СПД Резніков В.С., — 116 с.
- Ulevitch R.J., Tobias P.S. Recognition of Gram-negative bacteria and endotoxin by the innate immune system // Current Opinions in Immunology. — 2007. — № 11. — P. 19-22.
- Королюк М.А., Иванова Л.И., Майоров И.Г. Метод определения активности каталазы // Лабораторное дело. — 1988. — № 1. — С. 16-19.
- Стальная И.Д. Метод определения диеновой конъюгации ненасыщенных высших жирных кислот // Современные методы в биохимии. — М.: Медицина, 1977. — С. 63-64.
- Хейфец Л.Б., Абалакина В.А. Разделение форменных элементов крови человека в градиенте плотности верографин-фиколл // Лабораторное дело. — 1973. — № 10. — С. 579-581.
- Кульшин В.А., Яковлев А.А., Авиева С.Н. Улучшенный метод выделения липополисахаридов из грамотрицательных бактерий // Молекулярная генетика, микробиология и вирусология. — 1987. — № 5. — С. 44-46.
- Westphal O., Jann K. Bacterial lipopolysaccharides: extraction with phenol-water and further application of the procedure // Methods of Carbohydrate Chemistry. — 1965. — № 5. — 83-91.
- Стальная И.Д., Гаришвили Т.Г. Метод определения малонового диальдегида с помощью тиобарбитуровой кислоты // Современные методы в биохимии. — М.: Медицина, 1977. — С. 66-68.
- Чивари С., Чаба И., Секей И. Роль супероксиддисмутазы в окислительных процессах клетки и метод определения её в биологических материалах // Лабораторное дело. — 1985. — № 11. — С. 16-18.