Были разработаны и испытаны 6 вариантов контактно-сорбционного метода, все они показали эффективность их применения, которое оценивалось с учетом максимального показателя жизнеспособности. В качестве сорбента были взяты отечественные препараты «Тагансорбент» с ионами серебра, «Алтайсорбент» (ТОО «Сорбент», г. Усть-Каменогорск, РК).Также были отобраны наиболее доступные, простые в использовании и менее затратные варианты закладки на хранение контактно-сорбционным методом.
Введение
Актуальной остается проблема разработки комплексного подхода к консервации микроорганизмов, учитывающего как известные сведения о процессах, выработанных естественным отбором и способствующих сохранению микроорганизмов в природе, так и эмпирические достижения лабораторного хранения.
Длительное хранение клеток без утраты ценных свойств проводится методами, обеспечивающими существенное торможение протекающих у них жизненных процессов. Это достигается путем глубокого замораживания микроорганизмов или их высушивания из замороженного (лиофилизация) либо непосредственно из жидкого состояний (L-высушивание). Известно, что при длительном хранении культур микроорганизмов в музейных условиях, отличающихся от природных и производственных, некоторые свойства коллекционных культур ослабевают или даже утрачиваются [1, 2].
Одно из решений существующей проблемы по эффективному сохранению и развитию ресурсов промышленных коллекций заключается во внедрении методов хранения ценных культур современными технологиями с использованием субкультивирования контактно-сорбционным методом на различных носителях.
Успешность лабораторных программ консервации, несомненно, может быть повышена, если будут использоваться популяции клеток, реализующие свойственные им процессы «самоконсервации» либо индуцированные к этому соответствующими экспериментальными воздействиями с использованием различных инновационных методов хранения, в том числе субкультивирование с использованием контактно-сорбционного метода на различных носителях [3].
Материалы и методы
Объекты исследования: коллекционные культуры — бактерии, дрожжи, мицелиальные грибы, бациллы, лактобактерии, различные сорбенты отечественного производства. Методы исследования: микробиологические.
Оценка жизнеспособности и культурально-морфологических свойств микроорганизмов различных таксономических групп коллекции, заложенных на хранение субкультивированием контактно-сорбционным методом на носителях, путем их сравнения для определения преимуществ и недостатков того или иного носителя [4].
Культуральные признаки изучали на плотных и жидких питательных средах. Инкубировали в зависимости от таксономической группы при оптимальной температуре до 2-7 суток. Описание характера роста на жидких питательных средах оценивали по следующим признакам:
1) наличие пристеночного кольца;
2) наличие, характер, толщина поверхностной пленки;
3) характер и интенсивность мути;
4) цвет, структура, количество осадка.
Оценка показателя жизнеспособности культур микроорганизмов методом Miles&Misra и определение количества жизнеспособных клеток культуры методом последовательных посевов [5, 6].
Результаты и обсуждение
Нами были испытаны 6 вариантов контактно-сорбционного метода, все они показали эффективность их применения, которое оценивалось с учетом максимального показателя жизнеспособности. В качестве сорбента брали отечественные препараты «Тагансорбент» с ионами серебра, «Алтайсор-бент» (ТОО «Сорбент», г. Усть-Каменогорск, РК) на первом этапе хранения.
В ходе работы установлено, что показатель жизнеспособности стабилен при хранении во всех шести вариантах. Поэтому нами был проведен сравнительный анализ этапов подготовки каждого варианта с учетом доступности, простоты в использовании и менее затратных вариантов закладки на хранение контактно-сорбционным методом.
Недостатки 1-го варианта: на этапе стерилизации сорбента при температуре 110 °С тратилось много времени, т.е. 20-22 ч. Перед началом работ пробирки с сорбентом влаги охлаждали в течение 1-2 ч при температуре минус 20 °С, также проводили дополнительную процедуру, требующую времени.
Недостатки 2-го варианта: проведение контактно-сорбционного обезвоживания целевого продукта (микроорганизмы) на 2 этапе требуется охлаждать до минус 8-10 0C сорбентом с остаточной влажностью менее 1 % при массовом соотношении 1:10, требуется дополнительное время на охлаждение и регламентацию остаточной влажности.
Недостатки 4-го варианта: полученную клеточную суспензию смешивают с охлажденным до -18...-22 °С сорбентом в соотношении 1:6,5-7,5, проводится дополнительная процедура охлаждения. На этапе досушивания при комнатной температуре требуется по регламенту длительное время, т.е. 65-72 ч (до 3-х суток) в запечатанных пробирках.
Недостатки 5-го варианта: высушивали нелиофильным способом в течение 48 ч при температуре 50 °С, использовался адсорбционный метод сушки культуры, этот фактор (50 °С) отрицательно влиял на культуральные свойства, вызывая изменения S-формы колоний в R-форму, практически все штаммы дрожжей диссоциировали в данном варианте.
В силу этих причин для дальнейшей работы были отобраны наиболее доступные, простые в использовании и менее затратные варианты закладки на хранение контактно-сорбционным методом: 3 и 6, которые при текущем этапе работы, с учетом всех результатов и количества отработанной суспензии и защитной среды, были признаны эффективными.
В вариантах контактно-сорбционного метода также были отработаны следующие положения:
- Отработан объем суспензии (250 мкл суспензии микроорганизмов + 250 мкл 10 % молока), при внесении в адсорбент образуется минимум жидкости, при этом меньше времени уходит на сушку при использовании 3 и 6 вариантов.
- Количество адсорбента 200 мг является наиболее оптимальным для поглощения 500 мкл жидкости.
Также нами в ходе работы была выбрана наиболее упрощенная схема реактивации. Реактивацию после консервации методом КСО проводили введением в часть пробирок физиологического раствора, охлажденного до 2-4 °С, в часть пробирок неохлажденного физиологического раствора, с последующим высевом 0,1 мл содержимого на плотную питательную среду. При сравнении использованных физиологических растворов, охлажденного до 2-4 °С и неохлажденного, не установлено влияния разницы на результаты, поэтому мы исключили процедуру охлаждения физиологического раствора. В дальнейших исследованиях предусмотрена серия опытов по лиофилизации дубликатов культур вариантов, заложенных на хранение контактно-сорбционным методом.
Микроскопия препаратов, приготовленных из коллекционных микроорганизмов различных таксономических групп, заложенных на хранение контактно-сорбционным методом с использованием «Тагансорбента» и «Алтайсорбента» на 3-м и 6-м вариантах КСО, показала полное соответствие морфологии клеток исходным данным до закладки на хранение и паспортным данным по этому признаку.
Для продолжения экспериментального исследования на втором этапе нами были использованы отобранные варианты заложенных на хранение контактно-сорбционным методом: 3 и 6 с использованием «Тагансорбента» и «Алтайсорбента» выше приведенных коллекционных штаммов микроорганизмов различных таксономических групп. Была определена эффективность хранения микроорганизмов контактно-сорбционным методом через 3 месяца с их количественной оценкой ЖСП по мето ду Miles&Misra и методом последовательных посевов, контролем количественной оценки служил качественный показатель высева штамма после реактивации (табл. 1).
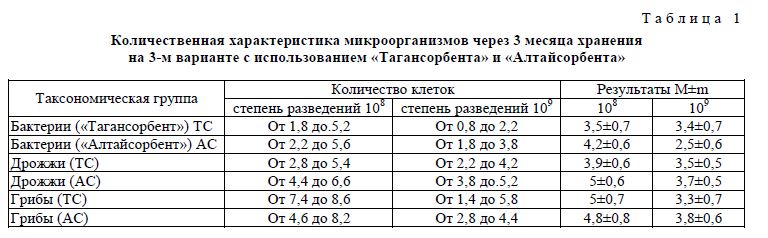
Окончательный вариант реактивации после консервации методом КСО включает: введение в пробирки с испытуемым штаммом физиологического раствора с последующим высевом 0,1 мл содержимого на соответствующую данному микроорганизму плотную питательную среду (см. рис.).
На рисунке показана количественная характеристика МКБ через 3 месяца хранения с использованием «Тагансорбента» и «Алтайсорбента» после реактивации и титрования.
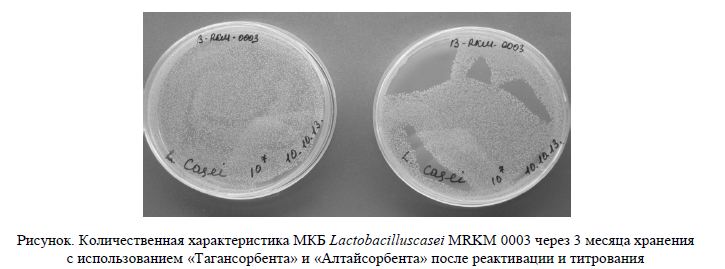
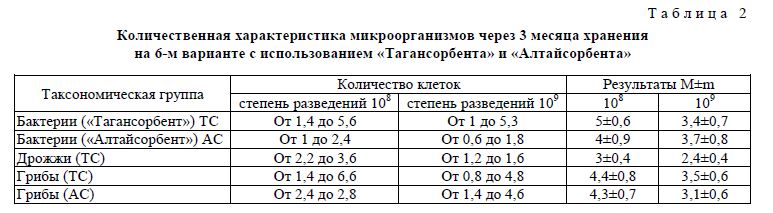
Рисунок. Количественная характеристика МКБ Lactobacilluscasei MRKM 0003 через 3 месяца хранения с использованием «Тагансорбента» и «Алтайсорбента» после реактивации и титрования
Результаты количественной и качественной оценок эффективности хранения коллекционных микроорганизмов различных таксономических групп контактно-сорбционным методом с использованием «Тагансорбента» и «Алтайсорбента» через 3 месяца, их культурально-морфологическая характеристика и анализ литературы по данной проблеме позволили нам сделать некоторые обоснования и требования при использовании данного метода.
- Сущность метода КСО заключается в обезвоживании микроорганизмов при контакте с сорбентом влаги, в результате чего микроорганизмы теряют воду и метаболические процессы резко замедляются.
- КСО с использованием «Тагансорбента» и «Алтайсорбента» позволяет консервировать и сохранять различные группы микроорганизмов без потери ими своих основных биологических свойств (морфологических и культуральных, изученных нами на этом этапе).
- Предпочтительнее использовать в качестве защитной при КСО минимальные среды, поскольку в них процессы метаболизма микроорганизмов идут с пониженными скоростями и поэтому промежутки между пересевами удлиняются.
- При использовании комплексной среды могут потребоваться более частые пересевы, связанные с ускоренным ростом микроорганизмов или накоплением конечного продукта метаболизма.
- Для уменьшения высыхания культур необходимо использовать пробирки с завинчивающимися крышками или резиновые пробки (если нет необходимости высушивания).
- Для уменьшения скорости метаболизма микроорганизмов культуры необходимо хранить в бытовом холодильнике при температуре 5-8 °С (кроме условий хранения при других показателях).
- Частоту пересевов определяют экспериментальным путем, стараясь проводить их как можно реже во избежание селекции вариантов.
- Используя эти меры предосторожности, можно сохранять большинство бактерий в течение 3-5 месяцев и более без пересева (сроки наблюдения на данном этапе).
- Реактивацию после консервации проводят введением в пробирку или флакон физиологического раствора с последующим высевом 0,1 мл содержимого на плотную питательную среду (через определенные сроки хранения).
- КСО не требует специального оборудования, значительных физических и экономических за-
трат.
Таким образом, контактно-сорбционный метод, не требующий специального оборудования, значительных физических и экономических затрат, позволяет консервировать и длительно сохранять различные группы микроорганизмов без потери ими своих основных биологических свойств.
Из изложенного выше можно сделать следующее заключение:
Были разработаны и испытаны 6 вариантов контактно-сорбционного метода, все они показали эффективность их применения, которое оценивалось с учетом максимального показателя жизнеспособности. В качестве сорбента были взяты отечественные препараты «Тагансорбент» с ионами серебра и «Алтайсорбент» (ТОО «Сорбент», г. Усть-Каменогорск, РК) на первом этапе хранения.
В ходе работы было установлено, что показатель жизнеспособности стабилен при хранении во всех шести вариантах контактно-сорбционного метода. При проведении сравнительного анализа этапов подготовки каждого варианта отобраны для дальнейших исследований 3-й и 6-й варианты.
При испытании различных вариантов контактно-сорбционного метода также были отработаны и оптимизированы следующие положения:
- отработан объем суспензии и защитной среды (250 мкл суспензии микроорганизмов + 250 мкл 10 % молока), при внесении в адсорбент образуется минимум жидкости, при этом меньше времени уходит на сушку при использовании отобранных вариантов;
- количество адсорбента 200 мг является наиболее оптимальным для поглощения 500 мкл жидкости;
- также нами в ходе работы была выбрана наиболее упрощенная схема реактивации после хранения на адсорбентах.
Выводы
- Заложены 50 штаммов микроорганизмов 5 таксономических групп на различные сроки хранения контактно-сорбционным методом с использованием препаратов «Тагансорбент» и «Алтайсор-бент» в качестве носителей.
- Проведено изучение качественных и количественных показателей 50 коллекционных штаммов промышленных микроорганизмов: бактерий, дрожжей, мицелиальных грибов, бацилл, лактобак-терий, заложенных на хранение контактно-сорбционным методом.
- Проведен сравнительный анализ этапов подготовки каждого варианта с учетом доступности, простоты в использовании и менее затратных вариантов закладки на хранение контактно-сорбцион-ным методом на адсорбентах, и отобраны для дальнейших исследований 3-й и 6-й варианты.
- КСО с использованием «Тагансорбента» и «Алтайсорбента» позволяет консервировать и сохранять различные группы микроорганизмов без потери ими своих основных биологических свойств (морфологических и культуральных, изученных нами на этом этапе).
- Предпочтительнее использовать в качестве защитной при КСО минимальные среды, поскольку в них процессы метаболизма микроорганизмов идут с пониженными скоростями и поэтому промежутки между пересевами удлиняются.
- Для уменьшения высыхания культур необходимо использовать пробирки с завинчивающимися крышками или резиновые пробки (если нет необходимости высушивания).
- Для уменьшения скорости метаболизма микроорганизмов культуры необходимо хранить их в бытовом холодильнике при температуре 5-8 °С (кроме условий хранения при других показателях).
Список литературы
- Лозина-Лозинский Л.К. Адаптация и устойчивость организмов и клеток к низким и сверхнизким температурам // Очерки по криобиологии — Л.: Наука, 1972. — 288 с.
- Maintenance of microorganisms: A manual of laboratory methods / Ed. by B.Kirsop, J.Snell. — London: Acad. Press, — 207 p.
- Porter J.N. Cultural conditions for antibiotic-producing microorganisms // Methods in enzymology. —Y.: Acad. Press, 1975. — Vol. 43: Antibiotics. — P. 3-23.
- Smith D. The preservation and maintenance of living fungi / D.Smith, A.H.S.Onions. Kew (Richmond); Surrey (England): Commonwealth Mycol. Inst. Publ., — 51 p.
- Бекер М.Е., Рапопорт А.И., Калакуцкий Л.В. Торможение жизнедеятельности клеток. — Рига: Зинатне, 1987. —240 с.
- Бузолева Л.С. Некультивируемые формы бактерийYersiniapseudotuberculosisпри периодическом культивировании // Бюл. экспериментальной биологии и медицины. — 2000. — Т. 129, № 4. —C. 444-447.