Были синтезированы 2,4-диоксо-1,4-дигидро-2Н-тиено[3,2-d]пиримидин-3-ил)карбоновые кислоты окислением соответствующих 2- тиоксо производных тиено[3,2-d]пиримидин-3-ил-карбоновых кислот раствором пероксида водорода в щелочной среде. Амидированием полученных карбоновых кислот с использованием N, N'-карбодиимидазола с первичными и вторичными аминами ситезированы целевые N-замещенные амиды 2,4-диоксо-1,4-дигидротиено[3,2-d]пиримидин-3-карбоновых кислот. Противомикробную активность полученных соединений изучали методом диффузии в агар. Исследованные целевые N-замещенные амиды 2,4-диоксо-1,4-дигидротиено[3,2-d]пиримидин-3-карбоновых кислот оказались активными по отношению к штаммам Staphylococcus aureus и Bacillus subtilis.
Актуальность проблемы. Эффективным направлением создания новых биологически активных веществ является конструирование и синтез гетероциклов, содержащих в своей структуре фармакофоры различной гетероциклического природы. Соединение в одной молекуле тиофенового и пиримидинового цикла приводит к расширению спектра фармакологической активности. Так, среди производных тиено[3,2-d]пиримидина найдены соединения, описанье как противомикробные и противовирусные [1, 2, 3, 4, 5] анальгезирующие и противовоспалительные [6], противоопухолевые [7, 8, 9], противопаразитарные [10, 11] средства, вещества для лечения нейродегенеративных заболеваний [12], лечения ожирения [13]. Поэтому синтез и изучение протимикробного действия производных тиено[3,2- d]пиримидина является актуальным.
Цель исследования. Оптимизация путей синтеза и исследование противомикробной активности N- замещенные амиды 2,4-диоксо-1,4-дигидротиено[3,2- d]пиримидин-3-карбоновых кислот.
Материалы и методы исследования. Все реагенты и растворители были получены из коммерческих источников. Температуры плавления были получены на устройстве Buchi B-520. 1Н ЯМР-спектры регистрировали спектрометром Bruker 170 Avance на частоте 200 МГц, 500 МГц (ДМСО-d6); TMS использовался как внутренний стандарт; химические сдвиги были приведены в шкале δ (м.д.). ТСХ проводили на алюминиевых пластинах, покрытых силикагелем (Merck, Kiesgel 60 F-254). Элементный анализ (N) осуществляли на приборе Euro EA-3000 фирмы EuroVector.
Методика синтеза (2,4-диоксо-1,4-дигидро-2Н-тиено[3,2- d]пиримидин-3-ил) карбоновых кислот 2 (а, b) описана нами в литературе [1].
(2,4-Диоксо-1,4-дигидро-2Н-тиено[3,2-d]пиримидин-3- ил)этановая кислота 2 (а) Выход 70%. Тпл. 168-170ºС. 1Н NMR, δ, ppm: 13.02 s (1Н, ОH); 11.80 s (1Н, NH); 8.08 d (1H, Н6); 6.94 d (1H, Н7); 4.50 s (2Н, СН2) Анал. для C8H6N2O4S: расч. N, 12.38; эксп. N, 12.39.
(2,4-Диоксо-1,4-дигидро-2Н-тиено[3,2-d]пиримидин-3- ил)пропановая кислота 2 (b). Выход 60%. Тпл. 192-194ºС. 1Н NMR, δ, ppm: 11.80 s (1Н, NH); 8.02 d (1H, Н6); 6.92 d (1H, Н7); 4.02-4.10 m (2Н, СН2); 3.20 s (1Н, ОH in exchange); 2.32-2.40 m (2Н, CН2). Анал. для C9H8N2O4S: расч. N, 11.66; эксп. N, 11.74.
Амиды (2,4-диоксо-1,4-дигидро-2Н-тиено[3,2-d]пиримидин- 3-ил)карбоновых кислот 3 (а-h) синтезированы за методикой, описаной ранее [14].
Изучение антимикробной активности. В соответствии с рекомендациями ВОЗ [15, 16] для оценки активности тестируемых соединений использовали тест-штаммы Staphylococcus aureus ATCC 25923, Esherichia coli ATCC 25922, Pseudomonas aeruginosa ATCC 27853, Proteus vulgaris ATCC 4636, Bacillis subtilis ATCC 6633, Candida albicans ATCC 653/885. Микробное нагрузка составляла 107 микробных клеток на 1 мл среды и устанавливалась по стандарту McFarland. Культуры выдерживают в течение 18-24 ч при 36ºC ± 1ºC. Для исследований использовали агар Мюллера- Хинтон (Дагестанский НИИ питательных сред). Соединения вводили методом диффузии в агар (лунками) в виде раствора в ДМСО в концентрации 100 мкг/мл в объеме 0,3 мл. При оценке новых антибактериальных веществ, а также при изучении антибиотикорезистентности штаммов применяли критерии размера зон задержки роста микроорганизмов вокруг лунки.
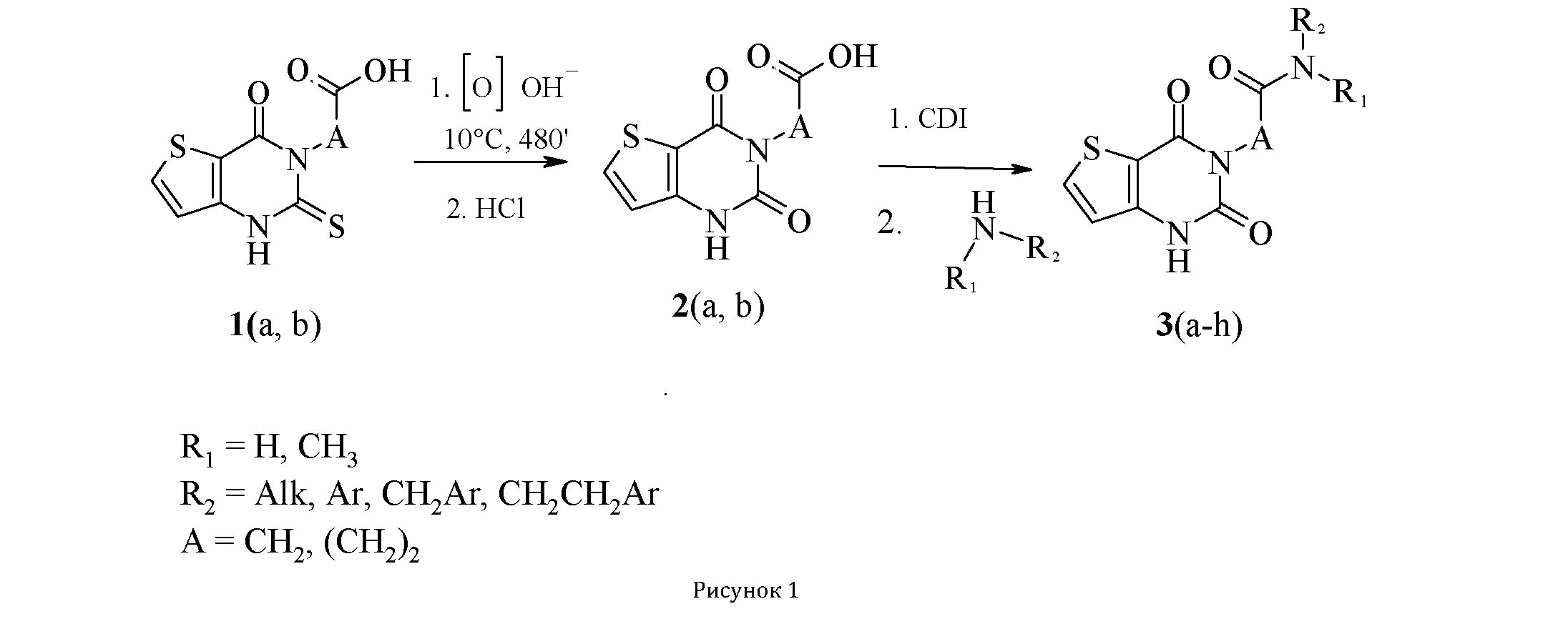
Результат исследования. Наличие в структуре синтезированных нами ранее [14] 4-оксо-2-тиоксо-1,4- дигидро-тиено[3,2-d]пиримидин-3-карбоновых кислот 1 (а, b) тиоамидного фрагмента предоставляет возможность проведения серии химических превращений с участием атома серы. Мы остановили свое внимание на реакции окисления соединений 1 (а, b) раствором пероксида водорода в щелочной среде (схема 1). Структура полученных соединений 2 (а, b) подтверждена данными 1Н ЯМР-спектроскопии и данными элементного анализа, чистота подтверждена методом тонкослойной хроматографии. Так, 1H ЯМР-спектры кислот 2 (а, b) характеризуются наличием сигналов протонов тиофенового кольца в виде двух дублетных сигналов протонов H-6 (δ 8.02-8.08 м.д.) и H-7 (δ 6.92-6.94 м.д.). Сигнал протона карбоксильной группы соединения 2 (а) находится в области слабых полей и проявляется в виде уширеного синглета при δ 13.02 м.д., сигнал протона карбоксильной группы соединения 2 (b) не проявляются за счет обмена с растворителем. Сигнал протона NH-группы - в виде синглета при δ 11.80 м.д. Мультиплетность и расположение сигналов остальных протонов полностью соответствуют предложенной структуре соединений.
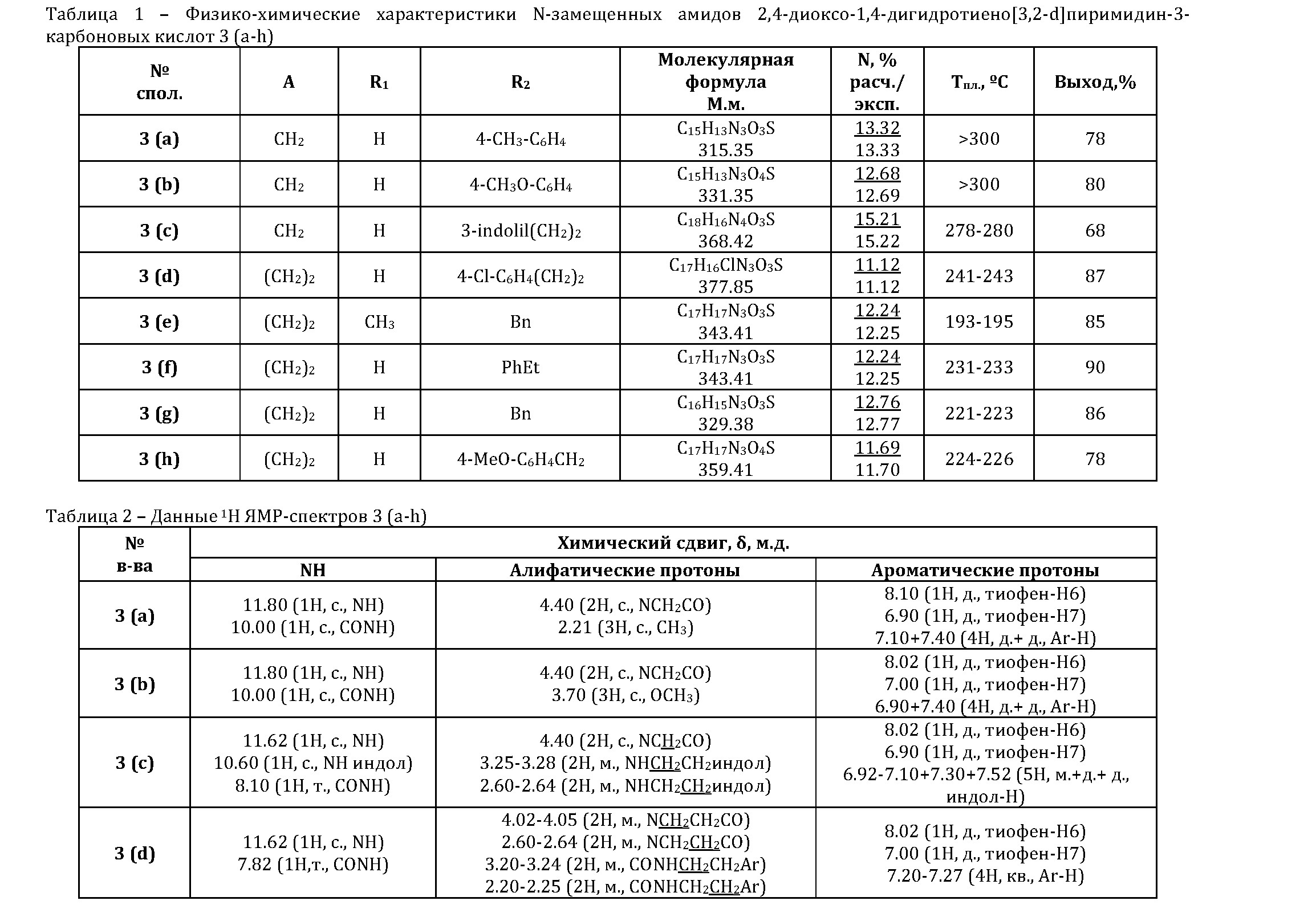
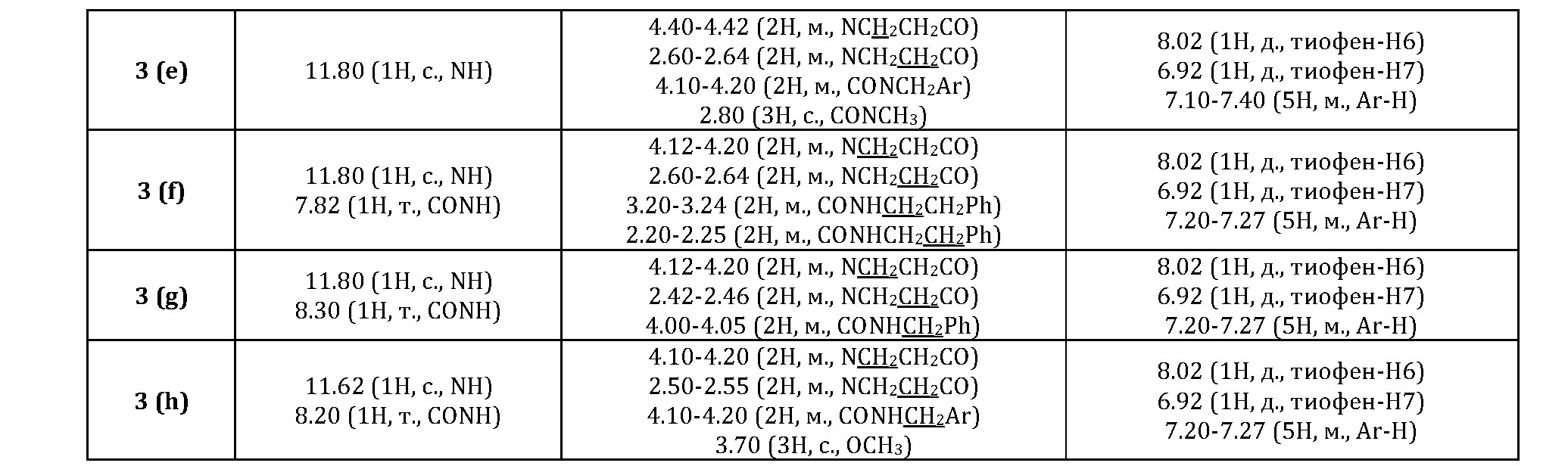
Амидирование 2,4-диоксо-1,4-дигидротиено[3,2- d]пиримидин-3-карбоновых кислот 2 (а, b) проводили с использованием N, N'-карбодиимидазола с первичными и вторичными аминами, что позволило получить целевые амиды 3 (а-h) с высокими выходами (68-90%) (схема 1). 1H ЯМР-спектры соединений 3 (а-d, f-h) характеризуются наличием сигнала протона амидной группы в области δ 7.82-10.00 м.д. соответствующей мультиплетности (таблица 1, 2).
С целью поиска биологически активных веществ в ряду N- замещенных амидов 2,4-диоксо-1,4-дигидротиено[3,2- d]пиримидин-3-карбоновых кислот 3 (а-h) проведено изучение противомикробного действия синтезированных соединений.
Противомикробной активностью соединений 3 (а-h)
изучали методом диффузии в агар. Антибактериальную активность оценивали путем измерения зон задержки роста соответствующего микроорганизма [15, 16]. При оценке противомикробной активности полученных соединений, а также при исследовании антибиотикотрезистентных штаммов применяли следующие критерии:
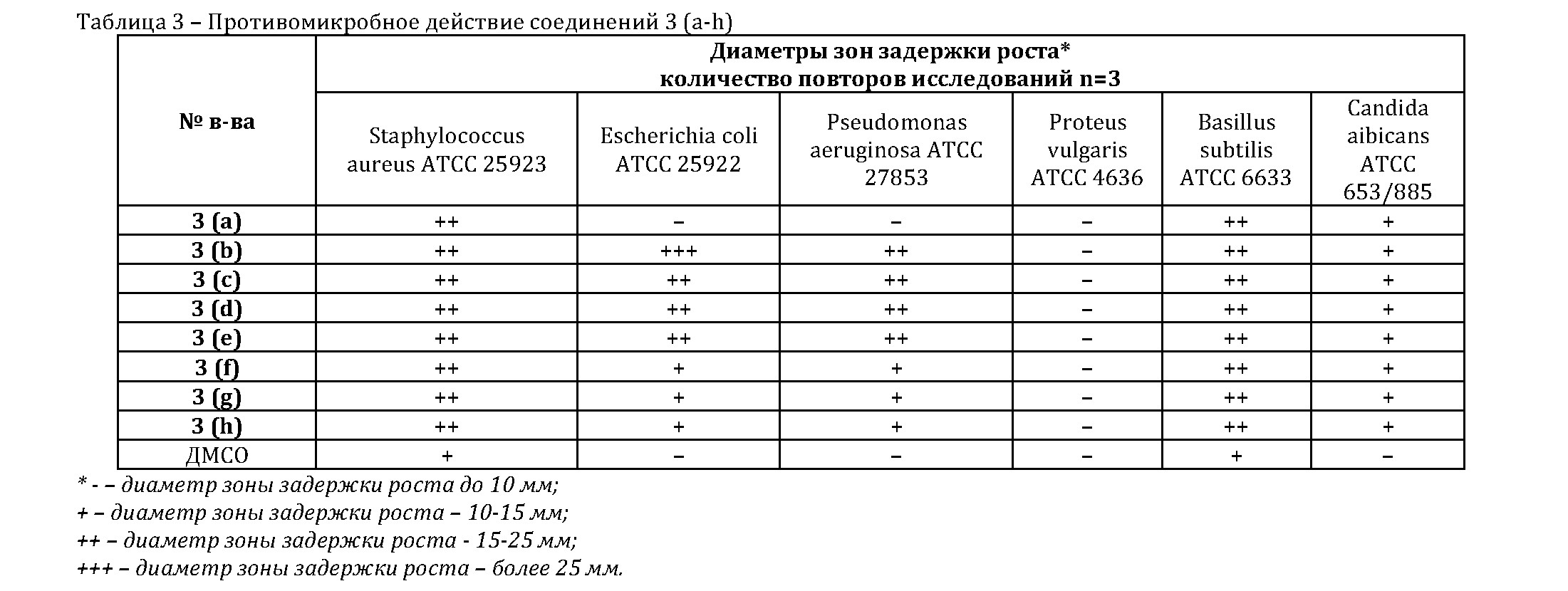
- отсутствие зоны задержки роста микроорганизма, а также задержка зоны, не превышающая 10 мм, указывают на отсутствие чувствительности микроорганизмов к соединению или недостаточной его концентрации;
- зона задержки роста диаметром 10-15 мм указывает на малую чувствительность культуры микроорганизма к исследуемой концентрации вещества;
- зона задержки роста диаметром 15-25 мм расцениваются как показатель чувствительности микроорганизма к исследуемому веществу; диаметр зоны задержки роста, который превышает 25 мм, свидетельствует о высокой чувствительности микроорганизмов к рассматриваемым веществам.
Данные результатов исследования противомикробной активности исследуемых образцов приведены в таблице 3.
Следует отметить, что все из исследованных соединений 3 (а-h) активны по отношению к Staphylococcus aureus, Basillus subtilis. К штамму Escherichia coli высокую активность имеют соединения 3 (b-e). Самый высокий показатель противомикробного действия имеет n-метоксибензиламид 2,4-диоксо-1,4-дигидротиено[3,2-d]пиримидин-3-этановой кислоты 3 (b). Соединения 3 (a, f-h) показали слабое противомикробное действие по отношению к штаммам Escherichia coli и Pseudomonas aeruginosa. Все исследованные соединения 3 (а-h) проявили слабое противогрибковое действие по отношению к Candida aibicans и отсутствие противомикробного действия по отношению к Proteus vulgaris.
Выводы. Новые N-замещенные амиды 2,4-диоксо-1,4- дигидротиено[3,2-d]пиримидин-3-карбоновых кислот были синтезированы и исследованы на противомикробную активность. Было установлено, что все полученные соединения активны против штаммов Staphylococcus aureus и Bacillus subtilis.
Конфликт интересов: Авторы данной статьи подтверждают отсутствие конфликта интересов, о котором необходимо сообщить.
СПИСОК ЛИТЕРАТУРЫ
- Tkachenko O.V., Vlasov S.V., Kovalenko S.M., Zhuravel' I.O., Chernykh V.P. Synthesis and antimicrobial activity 1-n-alkylated derivatives of 3-N-substituted 1Н-thieno[3,2-d]pirimidine-2,4-diones // Journal of Organic and Pharmaceutical Chemistry. - 2013. - Vol. 11, Iss. 4 (44). - P. 15-21.
- Ткаченко Е.В., Власов С.В., Журавель И.А., Коваленко С.Н., Черных В.П. Синтез и противомикробная активность 2-алкилтио-3-N- замещенных тиено[3,2-d]пиримидин-4(3H)-онов // Научные ведомости БелГУ. Медицина Фармация. - 2013. - № 25(168), Вып. 24/1. - С. 131-138.
- Manish S., Khyati P., Hansa P. Synthesis of thiazolidinones and azetidinones from hydrazinothieno[3,2-d]pyrimidines as potential antimicrobial agents // Indian J. Chem. Section B. - 1998. - Vol. 37В, №1. - P. 73-77.
- Kang D., Fang Z., Huang B., Lu X. et al. Structure-Based Optimization of Thiophene[3,2-d]pyrimidine Derivatives as Potent HIV-1 Nonnucleoside Reverse Transcriptase Inhibitors with Improved Potency against Resistance-Associated Variants // J. Med. Chem. - 2017. - Vol. 60, Iss. 10. - P. 4424-4443.
- Kang D., Fang Z., Li Z. et al. Design, Synthesis, and Evaluation of Thiophene[3,2-d]pyrimidine Derivatives as HIV-1 Non-nucleoside Reverse Transcriptase Inhibitors with Significantly Improved Drug Resistance Profiles // J. Med. Chem. - 2016. - Vol. 59, Iss. 17. - P. 7991-8007.
- Muraokaa T., Nakamurab M., Nishiharaa M. et al. Discovery of a potent and highly selective transforming growth factor β receptor- associated kinase 1 (TAK1) inhibitor by structure based drug design (SBDD) // Bioorg. Med. Chem. - 2016. - Vol. 24, Iss. 18. - P. 42064217.
- Kurasawa O., Oguro Y., Miyazaki T., et al. Identification of a new class of potent Cdc7 inhibitors designed by putative pharmacophore model: Synthesis and biological evaluation of 2,3-dihydrothieno[3,2-d]pyrimidin-4(1H)-ones // Bioorg. Med. Chem. - 2017. - Vol. 25, Iss.
- - P. 2133-2147.
- Zhan M., Deng Y., Zhao L. et al. Design, Synthesis, and Biological Evaluation of Dimorpholine Substituted Thienopyrimidines as Potential Class I PI3K/mTOR Dual Inhibitors // J. Med. Chem. - 2017. - Vol. 60, Iss. 9. - P. 4023-4035.
- Liu Z., Wang Y., Lin H. et al. Design, synthesis and biological evaluation of novel thieno[3,2-d]pyrimidine derivatives containing diaryl urea moiety as potent antitumor agents // Eur. J. Med. Chem. - 2017. - Vol. 85, Iss. 5. - P. 215-227.
- A. Cohena. P. Suzanneb, J.-Ch. Lancelot et al. Discovery of new thienopyrimidinone derivatives displaying antimalarial properties toward both erythrocytic and hepatic stages of Plasmodium // Eur. J. Med. Chem. - 2015. - Vol. 95. - P. 16-28.
- Gonzàlez Cabrera D., Douelle F., Manach C. et al. Structure - Activity Relationship Studies of Orally Active Antimalarial 2,4-Diamino- thienopyrimidines // Eur. J. Med. Chem. - 2015. - Vol. 58, Iss. 18. - P. 7572-7579.
- Dyck B., Branstetter B., Gharbaoui T. et al. Discovery of Selective Phosphodiesterase 1 Inhibitors with Memory Enhancing Properties // Eur. J. Med. Chem. - 2017. - Vol. 60, Iss. 8. - P. 3472-3483.
- Ahmad S., Washburn W.N., Hernandez A.S. et al. Synthesis and Antiobesity Properties of 6-(4-Chlorophenyl)-3-(4-((3,3-difluoro-1- hydroxycyclobutyl)methoxy)-3-methoxyphenyl)thieno[3,2-d]pyrimidin-4(3H)-one (BMS-814580): A Highly Efficacious Melanin Concentrating Hormone Receptor 1 (MCHR1) Inhibitor // J. Med. Chem. - 2016. - Vol. 59, Iss. 19. - P. 8848-8858.
- Ivachtchenko Al., Kovalenko S., Tkachenko O.V., Parkhomenko O. Synthesis of Substituted Thienopyrimidine-4-ones // J. Comb. Chem. - 2004. - Vol. 6, Iss. 4. - P. 573-583.
- Бактеріологічний контроль поживних середовищ. Інформаційний лист МОЗ Украïни №05.4.1/1670. - Киïв: 2001. - 48 с.
- Методичні рекомендацiï «Вивчення специфiчноï активності антимікробних лікарських засобів». - Киïв: 2004. - 38 с.