Рассчитаны следующие важные дескрипторы электронного строения имдазола и его производных, такие как: общая энергия молекулярной системы (Etot), стандартные энтальпии образования (∆fHo), энергии верхней занятой (EВЗМО) и нижней свободной (Енcмo) молекулярных орбиталей, зарядовые характеристики (q) на гетероатомах и Дипольные моменты (µ).Квантово-химические исследования позволили установить потенциальные активные центрымежмолекулярного взаимодействия реагентов в биосистемах и спрогнозировать биологическую активность препаратов для получения нового типа композитных материалов в биохимических и медико-биологических инженерных технологиях.
Введение. В настоящее время особую актуальность приобретают исследования, связанные с установлением связи структура-активность и направленные на решение одной из основных проблем фармации и фармакологии - выяснение зависимости между химическим строением веществ, их физико-химическими свойствами и биологической активностью. При этом важно выяснить, какие функциональные группы и особенности структуры определяют основные фармакологические эффекты исследуемых веществ [1].
Существует много подходов в исследованиях корреляций структура-действие для родственных соединений и установлении межрядовой связи. Более объективными из них являются факторы (дескрипторы), реализуемые в квантово-химическом подходе, так как именно анализ квантово-химических дескрипторов позволяет корректно установить связь структура-активность.
Квантово-химические расчёты, основанные на уравнениях квантовой механики, позволяют дать точное математическое описание экспериментально наблюдаемых внутри- и межмолекулярных взаимодействий, а также объяснить реакционную способность биоактивных веществ и предсказать возможные направления их использования в практической медицине[2-3].
Материалы и методы.
Для оптимизации геометрии и расчета дескрипторов электронного строения использован квантово-химический метод РМ3, в котором используется параметризация по термохимическим данным [4-6]. Для расчетов использовалось приближение Полака-Рибьера [7, 8].
Результаты квантово-химических расчетов предполагается в дальнейшем проанализировать в сочетании с результатами, полученными по компьютерной программе для прогноза спектра биологической активности РАSS [9].Эта программа, представленная на Web-сайте [10], позволяет предсказывать по структурной формуле соединения свыше 700 эффектов и механизмов их действия в качестве лекарственных веществ с точностью ~85%. Биологическая активность описывается в PASS качественным образом («да»/»нет»). Чем больше для конкретной активности величина Ра и чем меньше величина Pi, тем больше шанс обнаружить данную активность в эксперименте.
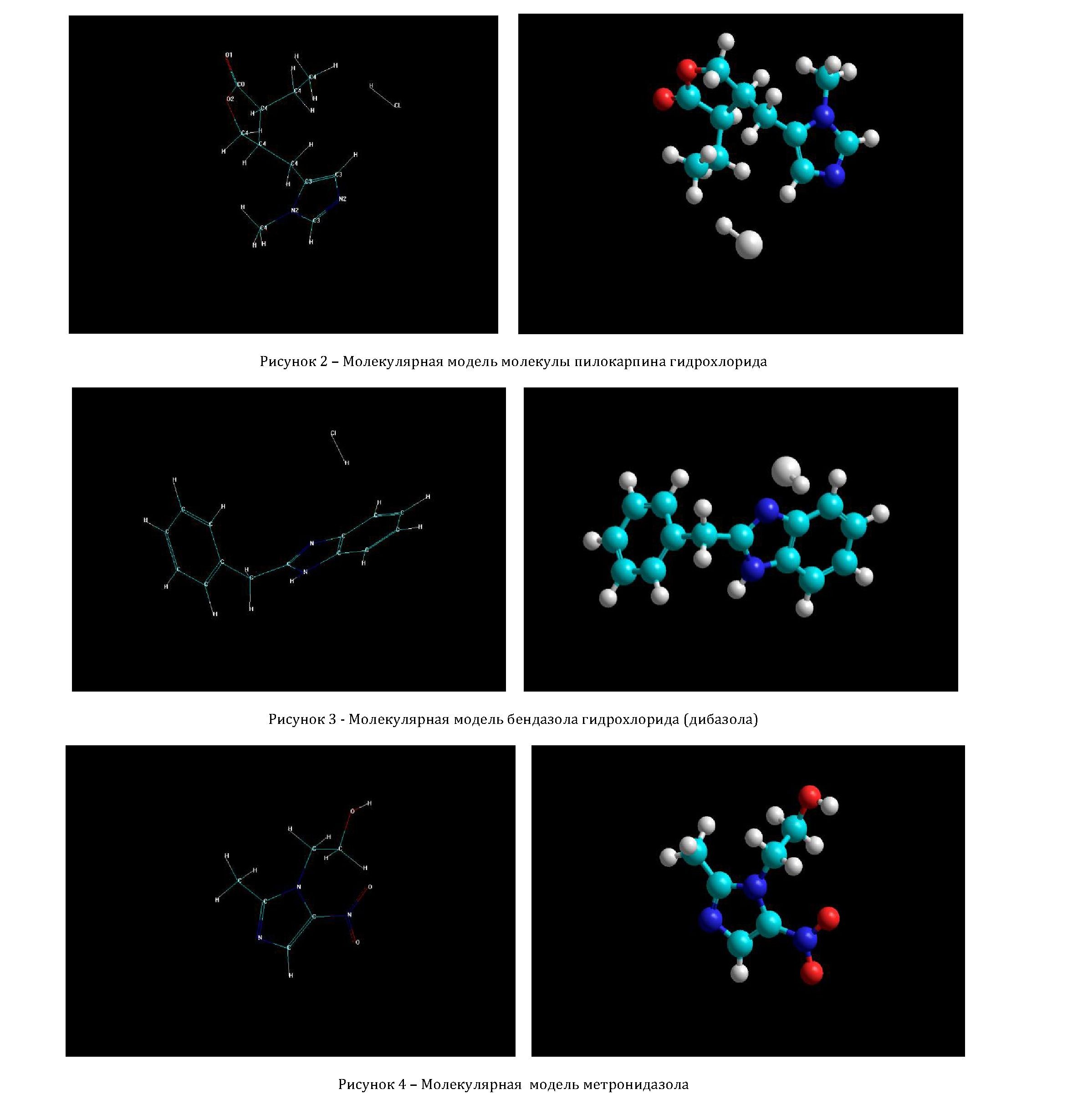
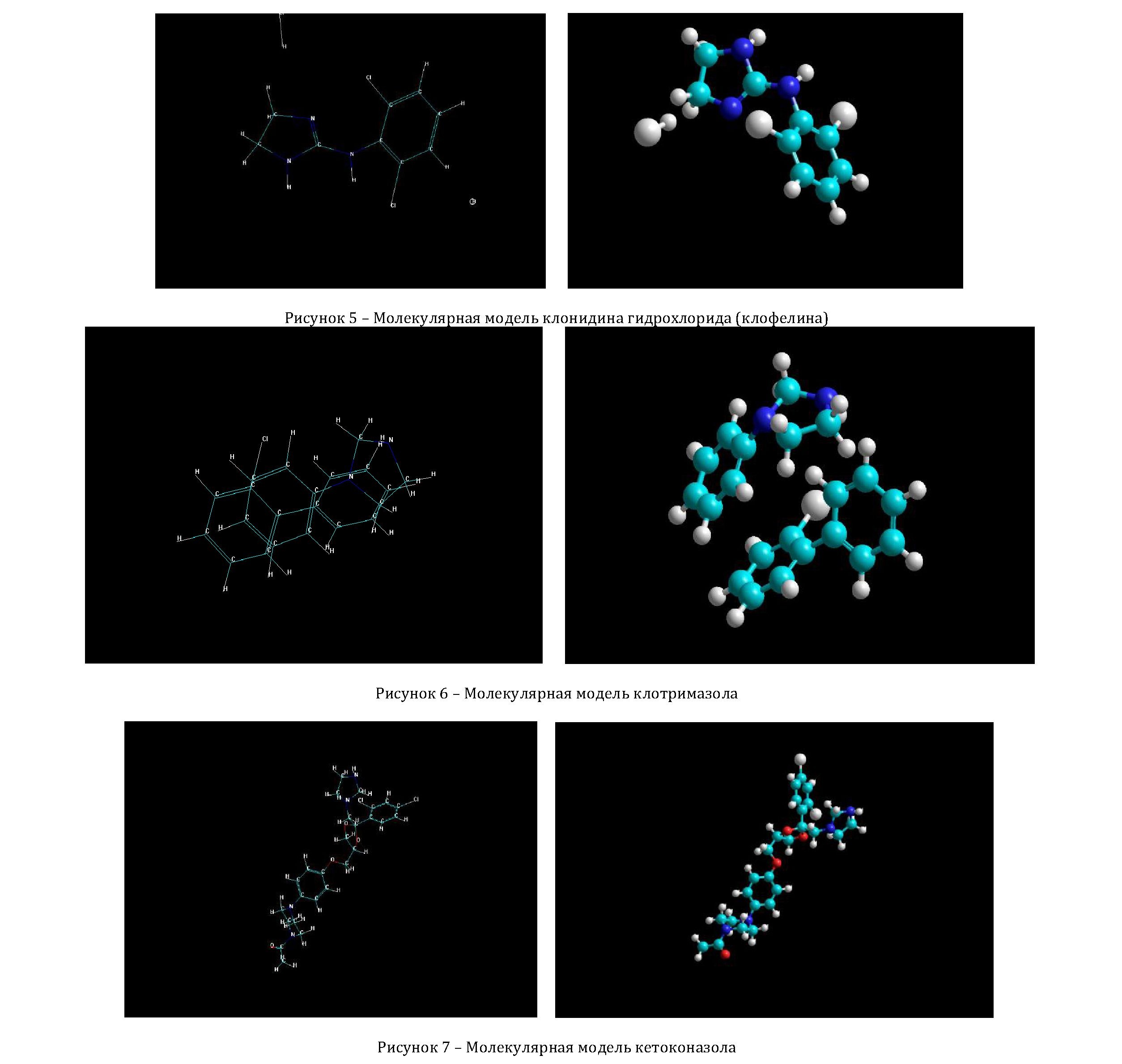
В качестве объектов исследования были взяты молекулярные модели следующих лекарственных веществ, производных имидазола: имидазол, бендазол, пилокарпина гидрохлорид, клонидина гидрохлорид, метронидазол, клотримазол, кетоконазол.
Результаты и обсуждение.
Имидазол проявляет, как известно, слабое физиологическое действие и является сравнительно малотоксичным [11]. Но степень физиологического действия и его направленность, как показывает медицинская практика, в значительной степени определяются природой заместителя, поэтому указанные выше производные имидазола обладают более высокой физиологической активностью. Известен ряд исследований, связанных с квантово-химическими расчетами структуры и прогнозированием биологической активности ряда тиокарбонил- и сульфанилбисазолов, а также производных имидазола с алкильными заместителями в иминогруппе [12-14].
Полученные с помощью графического драйвера изображения молекулярных моделей исследованных соединений, а также изображения моделей молекул с символами атомов в моделях представлены на рисунках 1-7.
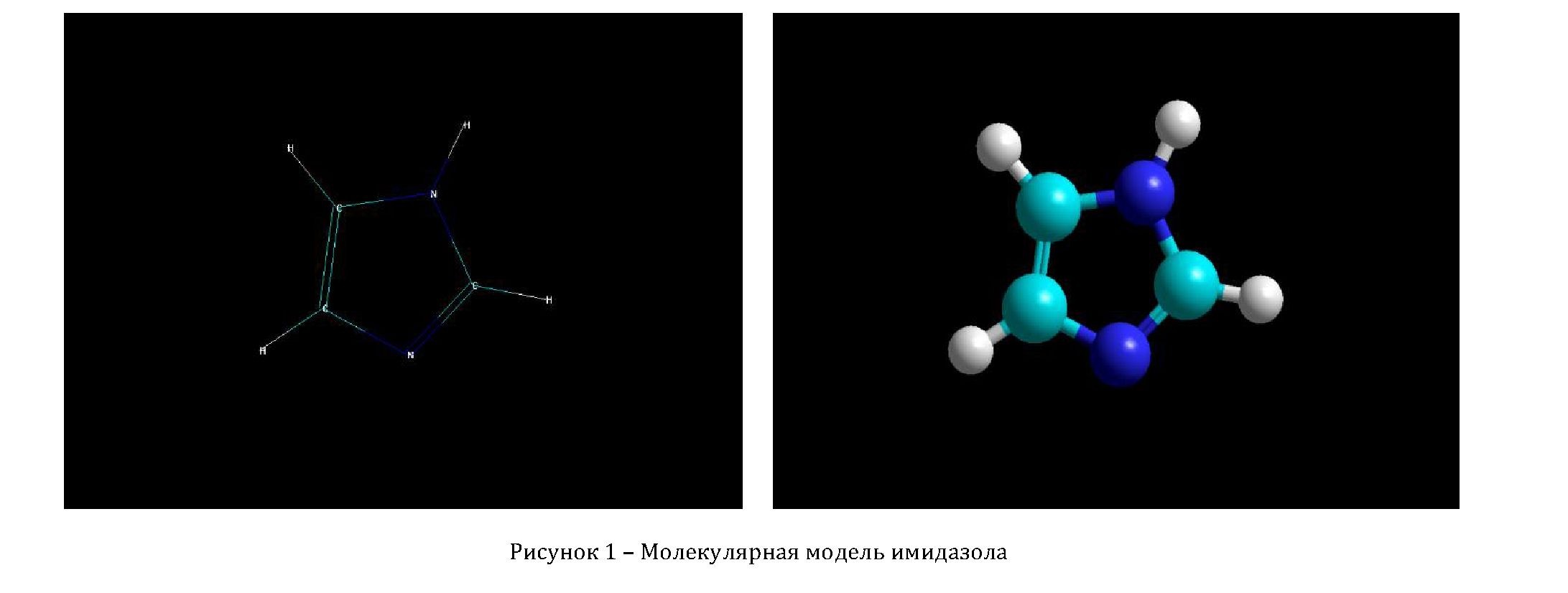
В качестве дескрипторов реакционной способности исследованных молекул были взяты следующие электронные характеристики: общая энергия молекулярной системы (Etot), энтальпия образования (∆fHo), энергии верхней занятой (EВЗМО) и нижней свободной (ЕНСМО) молекулярных орбиталей, зарядовые характеристики (q) на гетероатомах и дипольные моменты (μ) молекул в целом. Значения указанных параметров представлены в таблице 1.
|
Дескриптор |
Имидазол |
Бендазола гидрохлорид |
Пилокарпина гидрохлорид |
Кетоконазол |
Метронидазол |
Клонидина гидрохлорид |
Клотримазол |
|
Etot, ккал/моль |
-19599, 14 |
-3282,05 |
-56781,92 |
-6959,97 |
-51074,15 |
-61285,49 |
-79605,13 |
|
∆f Ho, ккал/ моль |
254,510 |
42,7221 |
-69,4265 |
-101,3512 |
-36,7243 |
9,2957 |
68,4544 |
|
Eвзmо, эВ |
-8,7207 |
-9,1086 |
-9,4041 |
-8,8089 |
-10,3453 |
-9,0335 |
-8,6042 |
|
Енсмо, эВ |
-2,3006 |
-0,3669 |
0,3943 |
-0,3824 |
-1,0556 |
-0,3215 |
-0,2806 |
|
μ, D |
5,802 |
3,644 |
6,949 |
4.605 |
3,941 |
3,776 |
2,149 |
|
q (C1) |
-0,1473 |
-0,1497 |
q (C8) -0,2954 |
q (C24) -0,0933 |
q (C6) -0,6695 |
q (C11) -0,0830 |
q (C1) -0,0847 |
|
q (C2) |
-0,3069 |
q (C> -0,1952 |
q (C7) -0,1325 |
q (C25) -0,1020 |
q (C7) 0,0208 |
q (C12) -0,0428 |
q (C4) -0,1013 |
Таблица 1 - Дескрипторы реакционной способности молекул лекарственных веществ, производных имидазола
Анализ значений дескрипторов, представленных в таблице 1, показывает, что лекарственные препараты, производные имидазола, характеризуются значительными по абсолютной величине отрицательными значениями общих энергий (Etot), что обусловлено значительным количеством электронов у атома азота, входящего в состав молекулы имидазола и его производных. Он имеет неподеленную пару электронов, которая делает его донором электронов и позволяет проявлять основность и быть активным центром. При сравнении данной характеристики наблюдается следующая закономерность: значение рассматриваемого параметра по абсолютной величине возрастает при переходе от клонидина гидрохлорида к бендазола гидрохлориду.
Энтальпия образования исследованных молекулярных моделей имидазола и его производных, характеризующая их термодинамическую стабильность, имеет различные по знаку и абсолютной величине значения. Её анализ показывает, что наиболее термодинамически стабильной является модель пилокарпина гидрохлорида, а наименее стабильной - модель клонидина гидрохлорида.
Расчет таких важных дескрипторов электронного строения как энергии высшей занятой (ВЗМО) и нижней свободной (НСМО) молекулярных орбиталей позволяет рассчитать энергетическую разницу между ними, которая дает возможность оценивать характер реакционного взаимодействия исследованных молекулярных моделей с биорецепторами при попадании в живой организм. Цифровое значение этой разницы имеет отрицательный знак, а по абсолютной её величине исследованные соединения можно расположить в следующий ряд:
|
q (Cs) |
-0,2390 |
q (C14) -0,0869 |
q (C14) -0,0869 |
q (C28) 0,0441 |
q (C8) -0,1612 |
q (C13) -0,1145 |
q (Cs) -0,1056 |
|
q (Nз) |
-0,1334 |
q (N1s) -0,1041 |
q (Ж) -0,1086 |
q (N26) -0,0662 |
q (N4) -0,1318 |
q (N8) -0,2333 |
q (N2) -0,0058 |
|
q (N4) |
0,1198 |
q (N16) 0,2500 |
q (N7) 0,2791 |
q (N27) -0,0099 |
q (Ns) 0,3903 |
q (N9) 0,0003 |
q (N3) -0,0861 |
|
q (C12) -0,0803 |
q (C1) -0,1166 |
q (C8) -0,0636 |
q (N3) 1,3820 |
q (C2) -0,0882 |
q (C6) -0,1513 |
||
|
q (C1) -0,1496 |
q (〇2) -0,3199 |
q (〇9) -0,2661 |
q (C9) -0,0415 |
q (C3) -0,0886 |
q (C7) -0,0705 |
||
|
q (C2) 0,0198 |
q (〇3) -0,2370 |
q (〇10) -0,2774 |
q (〇1) -0,6435 |
q (C4) -0,1000 |
q (C8) -0,1328 |
||
|
q (C3) -0,1034 |
q (C4) -0,0063 |
q (C11) 0,0426 |
q (〇2) -0,5927 |
q (Cs) -0,0767 |
q (C9) -0,0697 |
||
|
q (C4) -0,1070 |
q (C13) -0,0960 |
q (C10) -0,1769 |
q (C6) -0,0968 |
q (C10) -0,1531 |
|||
|
q (Cs) -0,1010 |
q (C14) -0,0593 |
q (C11) 0,0641 |
q (C7) -0,1357 |
q (C11) -0,0383 |
|||
|
q (C6) -0,0964 |
q (C15) -0,1284 |
q (C12) -0,2963 |
|||||
|
q (C16) 0,0784 |
|||||||
|
q (C17) -0,1643 |
|||||||
|
q (C18) -0,1048 |
пилокарпина гидрохлорид > метронидазол > бендазола гидрохлорид > кетоконазол > клонидина гидрохлорид >
клотримазол > имидазол
Анализ представленного ряда позволяет сделать вывод о том, что наиболее реакционноспособными будут первые четыре члена этого ряда, а малой реакционной способностью будет обладать имидазол.
Все исследованные молекулярные модели обладают значительными дипольными моментами (от 6,949 D для молекулы пилокарпина гидрохлорида до 2,149 D для молекулы клотримазола), что свидетельствует об антисимметричности их электронного строения и, следовательно, о значительной потенциальной реакционной способности.
Рассмотрение зарядового распределения в имидазольном кольце имидазола в зависимости от природы заместителей, присутствующих в молекулах его производных показывает следующее.
Наибольший по абсолютной величине отрицательный заряд в исходной модельной молекуле имидазола локализован на атоме С2. Значительный отрицательный заряд имеет также атом С5. Оба атома находятся в имидазольном кольце и именно они являются потенциальными центрами для электрофильной атаки. На атомах азота, присутствующих в имидазольном кольце, отрицательные заряды по величине значительно меньше, чем у его производных, что делает их менее реакционноспособными.
Введение в качестве заместителей в молекулу имидазола двух бензольных колец и переход, соответственно, к структуре бендазола гидрохлорида приводит к значительному уменьшению отрицательного заряда на
соответствующих атомах в имидазольном фрагменте и появлению отрицательного заряда на всех атомах углерода в бензольных фрагментах молекулы последнего. Анализ отрицательных по знаку значений зарядов на атомах имидазольного кольца свидетельствует о более высокой реакционной способности присутствующих в нем атомов углерода, которые также могут быть потенциальными активными центрами при межмолекулярных взаимодействиях.
В модельной молекуле пилокарпина гидрохлорида, содержащей в качестве заместителя 5-членное О- содержащее гетерокольцо, наибольший отрицательный заряд локализован на кислороде этого кольца и связанном с ним карбонильном кислороде, что свидетельствует об их повышенной реакционной способности по отношению к электрофильным реагентам. Значительный по абсолютной величине отрицательный заряд наблюдается и на одном из атомов углерода в имидазольном кольце.
В молекуле кетоконазола, содержащей в своем составе два бензольных кольца, N- и О-гетерокольца, а также атомы хлора в качестве заместителей и атом кислорода в качестве связующего кольца, реакционная способность имидазольного кольца резко падает. Наиболее реакционноспособными в этой молекуле становятся атомы кислорода, присутствующие в её структуре.
В молекуле метронидазола в качестве заместителей появляются метильный и этильный радикалы и NO2-группа. Это приводит к появлению достаточно высокого по абсолютной величине отрицательного заряда на атоме углерода в имидазольном кольце, находящемся в непосредственной близости от атома азота, связанного с этильным радикалом. Кроме того, значительный отрицательный заряд появляется на атоме азота в нитрогруппе. Поэтому эти два атома могут выступать потенциальными реакционными центрами для электрофильной атаки и проявлять биологическую активность.
Молекула клонидина гидрохлорида отличается от исходного имидазола наличием связанного с его кольцом через иминогруппу бензольным кольцом, в котором два атома водорода замещены на атомы хлора. Возникающее за счет наличия двух электронодонорных атомов хлора перераспределение электронной плотности приводит к заметному возрастанию отрицательного заряда на том атоме азота в имидазольном кольце, который не связан с бензольным кольцом и делает именно его наиболее реакционноспособным в рассматриваемой молекуле.
Наибольший по абсолютной величине отрицательный заряд в молекуле клотримазола, в структуре которого присутствуют в качестве заместителей три бензольных кольца, локализуется на атомах углерода в имидазольным кольце, что делает их наиболее реакционноспособными при межмолекулярных реакциях.
Молекула хлороводорода, присутствующая в рассмотренных гидрохлоридах производных имидазола ни в одной из рассмотренных структур не связана с атомами азота в имидазольном кольце, как это утверждалось ранее [12]. Протонирование имидазольного кольца во всех производных имидазола, содержащих гидрохлорид, происходит по одному из отрицательно заряженных атомов углерода в этом кольце.
Таким образом, проведенные квантово-химические исследования имидазола и его производных однозначно позволили установить наиболее потенциальные активные центры, которые могут принимать участие в межмолекулярных реакциях и объяснять причину их биологической активности. Кроме того, эти соединения могут быть использованы для получения нового типа композитных материалов в биохимических и медикобиологических инженерных технологиях.
Выводы.
Прогноз спектра биологической активности для исследованных препаратов, исследованных по компьютерной программе РАSS, показывает следующее:
- Имидазол обладает антиэкзематозной (0,940), противосеборейной (0,813), лейкопоэз стимулирующей (0,707) активностями, может применяться для лечения слизистых оболочек (0,728);
- Бендазола гидрохлорид обладает антиишемической (0,807), антивирусной (0,704), вазопротекторной (0,692) активностями, может выступать промотором инсулина, регулятором нуклеотидного обмена;
- Пилокарпина гидрохлорид проявляет свойства ингибитора цитохрома Р450, хемо- и радиопротектора;
- Кетоконазол проявляет антипротозойное (0,928), антибактериальное (0,733), противогрибковое (0,648) свойства, может быть рекомендован в качестве ингибитора цитохрома Р450;
- Метронидазол обладает противопротозойной: амебиоз (0,974), трихомониоз (0,971), противоинфекционной (0,856) активностями, может быть рекомендован в качестве стимулятора роста;
- Клонидина гидрохлорид можно применять для лечения слизистых оболочек (0,933), психических расстройств (0,781), ринитов (0,753), заболеваний почек (0,626), стеноза (0,625). Его можно рекомендовать как стимулятор функции почек (0,790), общий анестетик (0,740), релаксант скелетных мышц (0,619);
- Клотримазол обладает антигрибковыми свойствами: ингибитор CYP51 (0,979), CYP2E1 (0,977), можно применять для лечения болезни Боула (0,922), себореи (0,849), применять как противоинфекционное (0,798) и противопротозойное средства.
СПИСОК ЛИТЕРАТУРЫ
- Харкевич Д.А. Фармакология. - М.: ГЭОТАР-медиа, 2001. - 728 с.
- Хёльтье Х.-Д., Зиппль В., Роньян Д., Фолькерс Г. Молекулярное моделирование. Теория и практика. - М.: БИНОМ. Лаборатория знаний, 2010. - 318 с.
- Степанов Н.Ф. Квантовая механика и квантовая химия. - М.: УРСС, 2001. - 503 с.
- Srivastava A. K., Shukla N. Quantitative structure activity relationship (QSAR) studies on a series of imidazole derivatives as novel ORL1 receptor antagonists // Journal of Saudi Chemical Society. - 2013. - Т.17., №3. - С. 321-328.
- Minaev B. F., Kobzev G. I. Response calculations of electronic and vibrational transitions in molecular oxygen induced by interaction with noble gases // Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. - 2003. - Т.59., №14. - С. 3387-3410.
- Грибов Л.А., Муштакова С.П. Квантовая химия. - М.: Гардарики, 1999. - 340 с.
- Кларк Т. Компьютерная химия. - М.: Мир, 1990. - 197 с.
- Demaison J., Boggs J.E., Csaszar A.G. Equilibrium Molecular Structures From Spectroscopy to Quantum Chemistry. - Boston: PDF CRC Press, 2006. - 280 p.
- Поройков В.В., Лагунин А.А., Коборова О.Н., Захаров А.В., Филимонов Д.А. Роль биои хемоинформатики в создании лекарств, действующих на множественные мишени // Биотехнология: состояние и перспективы развития: Материалы IV Моск. междунар. конгресса. — М.: 2007. — С. 76-86.
- http:// www. ibmh. msk. su/ PASS.
- Беликов В.Г. Фармацевтическая химия. В 2 ч.: Учебн. пособие. - М.: МЕДпресс-информ, 2008. - 616 с.
- Петров Д.Ю., Трякин Ф.С., Зарубин Ю.П., Пурыгин П.П. Квантово-химические расчеты молекул ДУУ-тиокарбонил- и АА'- сульфонилбис азолов // Материалы XII междунар. научно-практ. конф. «Молодежьинаука: реальностьибудущее». - Невинномысск: 2009. - С.188-190.
- Srivastava A.K., Shukla N. Quantitative structure activity relationship (QSAR) studies on a series of imidazole derivatives as novel ORL1 receptor antagonists // J. Saudi Chem. Soc. - 2013. - Vol. 17. - P. 321-328.
- Wnuk M., Maszall M.P., Zapecka A. et.all. Prediction of antimicrobial activity of imidazole derivatives by artificial neural networs // Cent. Eur. J. Med. - 2013. - №8(1). - P. 1-15.